题目内容
11.实验室制备氢氧化铁胶体的方法是:向沸水中逐滴加入5-6滴饱和的三氯化铁溶液,呈现红褐色,停止加热.(请补充完整)反应的化学方程式为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.分析 将饱和三氯化铁溶液滴人沸水中来制取氢氧化铁胶体.
解答 解:实验室制备氢氧化铁胶体的方法是:加热烧杯中的水至沸腾,向沸水滴加几滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色,即停止加热,要注意实验过程不能用玻璃棒搅拌,否则溶液出现浑浊;当反应体系呈现红褐色,即制得氢氧化铁胶体,应立即停止加热,否则也容易出现浑浊,产生红褐色的氢氧化铁沉淀,往沸水中滴加饱和氯化铁溶液后,可稍微加热煮沸,但不宜长时间加热,反应原理为:FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl,
故答案为:呈现红褐色;FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl.
点评 本题考查离子方程式、胶体的制备,掌握相关的反应原理是解答的关键,题目难度不大.

练习册系列答案
相关题目
1.如图是298K时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )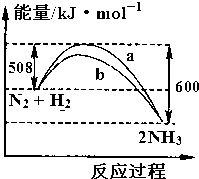

| A. | 该反应的热化学方程式为:N2+3H2?2NH3△H=-92 kJ•mol-1 | |
| B. | 向一密闭容器中加入1 molN2和3 molH2充分反应后,放出92 kJ热量 | |
| C. | b曲线可能是加入催化剂时的能量变化曲线 | |
| D. | 在N2+3H2?2NH3中,反应物的键能之和大于生成物的键能之和 |
2.下列说法正确的是( )
| A. | CH3COONa溶液中滴加少量浓盐酸后c(CH3COO-)增大 | |
| B. | 将硫酸铝和氯化铝溶液分别加热蒸干后灼烧,得到的固体都是氧化铝 | |
| C. | 中和体积与物质的量浓度都相同的HCl溶液和CH3COOH溶液消耗NaOH物质的量相同 | |
| D. | 中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗NaOH物质的量相同 |
19.把铁与铜的混合物放入稀HNO3中,反应后过滤,滤出的固体物质投入盐酸中无气体放出,则滤液里一定含有的金属盐是( )
| A. | Cu(NO3)2 | B. | Fe(NO3)3 | C. | Fe(NO3)2 | D. | Fe(NO3)2和Cu(NO3)2 |
6.下列离子方程式书写正确的是( )
| A. | 钠与水反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 用小苏打治疗胃酸过多:HCO${\;}_{3}^{-}$+H+═H2O+CO2↑ | |
| C. | 石灰石与盐酸反应:CO32-+2 H+═H2O+CO2↑ | |
| D. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag |
3. 已知某温度时CH3COOH的电离平衡常数为K.该温度下向20mL0.1mol/LCH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中正确的是( )
已知某温度时CH3COOH的电离平衡常数为K.该温度下向20mL0.1mol/LCH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中正确的是( )
 已知某温度时CH3COOH的电离平衡常数为K.该温度下向20mL0.1mol/LCH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中正确的是( )
已知某温度时CH3COOH的电离平衡常数为K.该温度下向20mL0.1mol/LCH3COOH溶液中逐滴加入0.1mol/L NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中正确的是( )| A. | a 点表示的溶液中c(CH3COO-)>10-3mol/L | |
| B. | b 点表示的溶液中c(Na+)>c(CH3COO-) | |
| C. | c 点表示CH3COOH和NaOH恰好反应完全 | |
| D. | b、d 点表示的溶液中$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$均等于K |
 实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应:
实验室制备1,2-二溴乙烷的反应原理是先用乙醇制备出乙烯,再将乙烯通入溴水中发生如下反应: