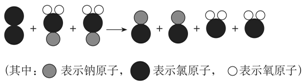
题目内容
8.下列物质属于共价化合物的是( )| A. | NH4Cl | B. | MgO | C. | H2O | D. | CaCl2 |
分析 含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,据此分析解答.
解答 解:A.氯化铵中铵根离子和氯离子之间存在离子键、N-H原子之间存在共价键,为离子化合物,故A错误;
B.MgO中镁离子和氧离子之间只存在离子键,为离子化合物,故B错误;
C.水分子中H-O原子之间只存在共价键,为共价化合物,故C正确;
D.CaCl2中钙离子和氯离子之间只存在离子键,为离子化合物,故D错误;
故选C.
点评 本题考查离子化合物和共价键化合物判断,为高频考点,明确物质构成微粒及微粒之间作用力是解本题关键,不能根据是否含有金属元素判断离子键,如氯化铝中只含共价键,为易错点.

练习册系列答案
相关题目
18.下列化学方程式不正确的是( )
| A. | 乙醇与浓氢溴酸反应:CH3CH2OH+HBr $\stackrel{△}{→}$CH3CH2Br+H2O | |
| B. | 溴乙烷与氢氧化钠溶液共热:CH3CH2Br+NaOH$\stackrel{△}{→}$CH3CH2OH+NaBr | |
| C. | 苯酚钠溶液中通入少量二氧化碳: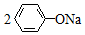 +CO2→ +CO2→ +Na2CO3 +Na2CO3 | |
| D. | 蔗糖在稀硫酸作用下水解:C12H22O11(蔗糖)+H2O$→_{△}^{稀硝酸}$C6H12O6(葡萄糖)+C6H12O6(果糖) |
19.下列物质的电离方程式书写正确的是( )
| A. | Na2SO4═Na++SO42- | B. | Ba(OH)2═Ba2++(OH)22- | ||
| C. | CH3COOH═CH3COO-+H+ | D. | NH4Cl═NH4++Cl- |
16.下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 组别 物质 | 甲 | 乙 | 丙 |
| A | Al2O3 | H2SO4 | NaOH |
| B | NO2 | HNO3 | NH3 |
| C | SiO2 | HF | NaOH |
| D | SO2 | Ca(OH)2 | NaHCO3 |
| A. | A | B. | B | C. | C | D. | D |
3.下列图示实验能达到实验目的是( )
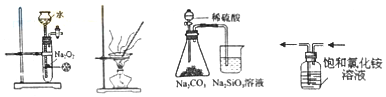

| A. | 制备少量O2 | B. | 制备无水氯化铁 | ||
| C. | 比较元素非金属性强弱 | D. | 收集氨气 |
13.下列离子方程式书写正确的是( )
| A. | 金属铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O | |
| C. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| D. | 铜跟稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O |
20.下列反应能够发生:
H2SO3+I2+H2O=H2SO4+2HI,2FeCl3+2HI=2FeCl2=2HCl+I2
3FeCl2+4HNO3=2FeCl3+Fe(NO3)3+2H2O+NO↑
由此判断下列有关物质还原性由强到弱的顺序正确的是( )
H2SO3+I2+H2O=H2SO4+2HI,2FeCl3+2HI=2FeCl2=2HCl+I2
3FeCl2+4HNO3=2FeCl3+Fe(NO3)3+2H2O+NO↑
由此判断下列有关物质还原性由强到弱的顺序正确的是( )
| A. | I->Fe2+>H2SO3>NO | B. | NO>Fe2+>H2SO3>I- | ||
| C. | Fe2+>I->H2SO3>NO | D. | H2SO3>I->Fe2+>NO |
13.下列有关化学用语表示正确的是( )
| A. | K+的结构示意图: | |
| B. | B、基态氮原子的电子排布图 | |
| C. | 水的电子式: | |
| D. | D、基态铬原子(24Cr)的价电子排布式:3d44s2 |