题目内容
电解原理在化学工业中有着广泛的应用。右图是一个电解池,a为电解液,x和y是两块电极板,通过导线与直流电源相连。回答下列问题,

(1)若X 和Y 为惰性电极,a 为饱和的氯化钠溶液,则电解池中Y电极反应式 __________________________,检验该电极反应产物的方法是_______________________________________________________。
(2)若X 和Y分别为石墨和铁,a 为饱和的氯化钠溶液,则点解过程中生成地 白色固体物质为________________________。将该物质露置在空气中,可观察到得现象为
__________________________________________________________。
(3)某同学做该实验时用铅蓄电池做电源,已知铅蓄电池的工作原理为Pb + PbO2 +2H2SO4![]() 2PbSO4+2H2O,则该蓄电池的负极反应式为_______________________________.
2PbSO4+2H2O,则该蓄电池的负极反应式为_______________________________.
若反应过程中转移的电子为0.1mol,则反应中电池内消耗的硫酸为______________.
(1)2C1-![]() Cl2+2e- 将湿润的淀粉碘化钾试纸靠近Y极支管口,试纸变蓝,说明有氯气生成
Cl2+2e- 将湿润的淀粉碘化钾试纸靠近Y极支管口,试纸变蓝,说明有氯气生成
(2)Fe(OH)2白色固体迅速变为灰 绿色,最终变为红褐色。
(3)Pb+S042-![]() PbS04+2e- 0.1mol
PbS04+2e- 0.1mol

练习册系列答案
相关题目
 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题: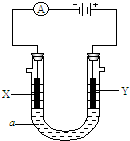 (I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.
(I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2. 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.