题目内容
19.H-C≡C-H中碳原子采取sp杂化,碳-碳三键之间有一个手拉手的σ键和两个肩并肩的π键.分析 根据价层电子对互斥理论确定杂化类型,价层电子对个数=σ键个数+孤电子对,σ键是轴对称的,π键是镜像对称,σ键头碰头重叠,π键肩并肩重叠,σ键重叠程度大,σ键更稳定,以此来解答.
解答 解:CH≡CH分子中每个C原子含有2个σ键和2个π键,价层电子对个数是2,碳原子采取sp杂化,σ键和π键都是共价键,σ键是由电子“头碰头”重叠形成的,是轴对称的,π键肩并肩重叠是镜像对称,σ键重叠方式大,比π键更稳定,所以碳-碳三键之间有一个手拉手的σ键,和两个肩并肩的π键.
故答案为:sp;σ;π.
点评 本题考查杂化类型、共价键的形成及类型,为高频考点,熟练应用价层电子对互斥理论、把握共价键的形成原因为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
10.下列有关海水资源综合利用的说法错误的是( )
| A. | 从海水中可以得到NaCl电解熔融NaCl可制备金属钠 | |
| B. | 海水蒸发制海盐的过程中不涉及化学变化 | |
| C. | 从海水中提溴、碘、镁单质,都利用了氧化还原反应 | |
| D. | 利用潮汐发电是将化学能转化为电能 |
7.用如图装置进行实验,能达到相应实验目的是( )
| A. | 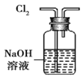 用装置除去Cl2中含有的少量HCl气体 | |
| B. | 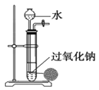 用装置制取少量O2时,能做到“随开随停” | |
| C. | 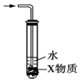 若装置中X为CCl4,则可用于吸收NH3或HCl | |
| D. |  用装置比较氯、碳、硅三种元素的非金属性强弱 |
14.下列说法可充分说明P(g)+Q(g)?S(g)+R(g),在恒温下,恒容密闭容器中的反应已达平衡的是( )
| A. | 容器里P、Q、R、S四种物质共存 | |
| B. | 容器里气体总物质的量不再改变 | |
| C. | 容器内气体压强、密度不随时间变化 | |
| D. | 单位时间内生成nmol P同时生成nmol S |
4.下列反应属于取代反应的是( )
| A. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| B. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| C. | CH3CH=CH2+Br2→CH3CHBrCH2Br | |
| D. | CHCl3+HF→CHFCl2+HCl |
11.在一定温度下,反应2XY(g)?X2(g)+Y2(g)达到平衡的标志是( )
| A. | 单位时间内生成n mol X2,同时生成n mol XY | |
| B. | 单位时间内生成n mol X2,同时生成n mol Y2 | |
| C. | 单位时间内生成2n mol XY,同时生成n mol Y2 | |
| D. | 容器内总压强不随时间变化 |
8.在理论上不能用于设计原电池的化学反应是( )
| A. | Al(OH)3(s)+NaOH(aq)═NaAlO2(aq)+2H2O(aq)△H<0 | |
| B. | CH3CH3OH(l)+3O2(g)-→2CO2(g)+3H2O(l)△H<0 | |
| C. | CO2(g)+C(g)═2CO(g)△H>0 | |
| D. | H2(g)+Cl2(g)═2HCl(g)△H<0 |