题目内容
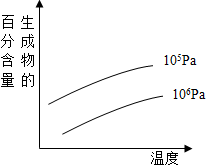 由可逆反应测绘出的图象如图所示,纵坐标为生成物在平衡体系中的百分含量,下列对该反应判断正确的是( )
由可逆反应测绘出的图象如图所示,纵坐标为生成物在平衡体系中的百分含量,下列对该反应判断正确的是( )| A、反应物中一定有气体 |
| B、生成物中一定无气体 |
| C、正反应一定是放热反应 |
| D、正反应一定是吸热反应 |
考点:反应热和焓变,化学平衡建立的过程
专题:
分析:“定一议二”:温度不变时,增大压强,生成物的百分含量降低,说明平衡逆向移动,逆向为体积缩小方向,而题中未给出具体的可逆反应,但是可以确定生成物中一定有气体,压强不变时,升高温度,生成物的百分含量增大,说明平衡正向移动,正向为吸热反应.
解答:
解:根据图示可以看出:压强不变,温度升高,产物的百分含量增大,所以平衡正向移动,反应是吸热的,温度不变,压强增大,产物的百分含量减小,所以平衡逆向移动,逆向为体积缩小方向,而题中未给出具体的可逆反应,但是可以确定生成物中一定有气体.
故选D.
故选D.
点评:本题考查学生影响化学平衡移动的因素:温度、压强,注意“定一议二”法的应用,难度中等.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、检验Cl-离子的试剂是硝酸银溶液和稀硝酸 |
| B、检验SO42-离子的试剂一般用氯化钡溶液和稀盐酸 |
| C、检验CO32-离子的试剂用盐酸和澄清石灰水 |
| D、在某溶液中加入BaCl2溶液产生白色沉淀,证明溶液中有SO42- |
如表除杂所选用的试剂及操作方法均正确的组合是(括号内为杂质)( )
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | I2(H2O) | CCl4 | 萃取、分液 |
| B | CO2(CO) | O2 | 点燃 |
| C | Zn (Cu) | 稀硫酸 | 过滤 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A、A | B、B | C、C | D、D |
抗生素能抑制或杀灭细菌、霉菌、支原体、衣原体等微生物,它的使用帮助人类战胜了多种疾病.关于抗生素的使用,下列说法正确的是( )
| A、当周围有人感染埃博拉病毒(EBOV)时,可以吃些抗生素以防被传染 |
| B、上呼吸道感染、咽痛等病毒疾病应该使用抗生素治疗 |
| C、抗生素在治病的同时也有副作用,没有一种抗生素是绝对安全而无副作用的 |
| D、使用某抗生素一两天后病情没有明显好转,应尽快换用其他抗生素 |