题目内容
(1)1g CH4燃烧时生成CO2与液态H2O,放出55.6kJ的热量,写出甲烷的燃烧热热化学方程式 .
(2)分别写出甲烷燃料电池在碱性条件下的负极反应 .
(2)分别写出甲烷燃料电池在碱性条件下的负极反应
考点:热化学方程式,电极反应和电池反应方程式
专题:化学反应中的能量变化,电化学专题
分析:(1)根据热化学方程式的书写方法可知,化学计量数与反应热成正比,并注意标明物质的聚集状态来解答,注意燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量;
(2)甲烷燃料电池甲烷在负极失电子,在碱溶液中生成碳酸根离子,依据电荷守恒配平书写电极反应.
(2)甲烷燃料电池甲烷在负极失电子,在碱溶液中生成碳酸根离子,依据电荷守恒配平书写电极反应.
解答:
解:(1)1g CH4燃烧时生成CO2与液态H2O,放出55.6kJ的热量,燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,则16g甲烷燃烧生成二氧化碳和液态水放热889.6kJ,热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=889.6kJ/mol;
故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=889.6kJ/mol;
(2)甲烷燃料电池甲烷在负极失电子,在碱溶液中生成碳酸根离子,甲烷燃料电池在碱性条件下的负极反应为:CH4-8e-+10OH-=CO32-+7H2O;
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=889.6kJ/mol;
(2)甲烷燃料电池甲烷在负极失电子,在碱溶液中生成碳酸根离子,甲烷燃料电池在碱性条件下的负极反应为:CH4-8e-+10OH-=CO32-+7H2O;
故答案为:CH4-8e-+10OH-=CO32-+7H2O;
点评:本题考查了热化学方程式书写方法和注意问题,原电池原理分析,电极反应书写,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列叙述是某同学做完铜锌原电池实验后得出的结论和认识,正确的是( )
| A、构成原电池正极和负极的材料必须是两种金属 |
| B、由铜锌作为电极与硫酸铜溶液组成的原电池中,铜是负极 |
| C、电流通过硫酸溶液,SO42-向正极移动 |
| D、铜锌原电池工作时,若有13g锌被溶解,电路中就有0.4mol电子通过 |
下列离子方程式正确的是( )
| A、在硫酸亚铁溶液中加入稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | ||||
B、MnO2与浓盐酸反应制取Cl2:MnO2+4HCl(浓)
| ||||
| C、过量的KHSO4与Ba(OH)2溶液反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | ||||
| D、向稀氢氧化钠溶液中通入少量CO2:OH-+CO2═HCO3- |
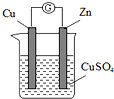 某实验兴趣小组按如图装置实验后,所记录内容合理的是( )
某实验兴趣小组按如图装置实验后,所记录内容合理的是( )| 实验 记录 | ①Cu为正极,Zn为负极; ②Zn质量减少,Cu质量不变; ③SO42- 向Cu极移动; ④电子流方向是:由Zn经导线流入Cu片; ⑤Zn电极发生还原反应; ⑥正极反应式:Cu2++2e-═Cu |
| A、①④⑥ | B、②③④ |
| C、①②⑤ | D、③⑤⑥ |
下列物质一定属于同系物的是( )


| A、⑤⑦ | B、④⑥ | C、⑥⑧ | D、①③ |

 用如图所示装置进行中和热测定实验,请回答下列问题:
用如图所示装置进行中和热测定实验,请回答下列问题: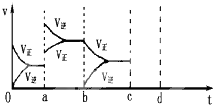 如图表示在密闭容器中反应:CO2(g)+C(s)?2CO(g)△H>0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是
如图表示在密闭容器中反应:CO2(g)+C(s)?2CO(g)△H>0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是

 (R为烃基)
(R为烃基) 反应合成聚碳酯的化学方程式
反应合成聚碳酯的化学方程式