题目内容
能形成高分子化合物的反应类型是( )
| A、消去反应 | B、复分解反应 |
| C、置换反应 | D、聚合反应 |
考点:聚合反应与酯化反应
专题:有机反应
分析:消去反应是指在一定条件下,有机物脱去小分子生成含有不饱和的有机物的反应;
复分解反应为两种化合物反应生成两种新的化合物的反应;
置换反应为单质与化合物反应生成新的单质和化合物的反应;
聚合反应:由相对分子质量小的化合物分子相互结合成相对分子质量大的高分子的反应叫做聚合反应,根据以上概念进行判断.
复分解反应为两种化合物反应生成两种新的化合物的反应;
置换反应为单质与化合物反应生成新的单质和化合物的反应;
聚合反应:由相对分子质量小的化合物分子相互结合成相对分子质量大的高分子的反应叫做聚合反应,根据以上概念进行判断.
解答:
解:A.消去反应为有机物脱去小分子形成不饱和有机物的反应,如乙醇通过消去反应生成乙烯,该反应中不会生成高分子化合物,故A错误;
B.复分解反应为无机反应类型,反应中不会生成高分子化合物,故B错误;
C.置换反应为单质与化合物反应生成新的单质和化合物的反应,不会生成高分子化合物,故C错误;
D.聚合反应分为加聚反应和缩聚反应,反应中生成高分子化合物,故D正确;
故选D.
B.复分解反应为无机反应类型,反应中不会生成高分子化合物,故B错误;
C.置换反应为单质与化合物反应生成新的单质和化合物的反应,不会生成高分子化合物,故C错误;
D.聚合反应分为加聚反应和缩聚反应,反应中生成高分子化合物,故D正确;
故选D.
点评:本题考查了常见反应类型及反应产物的判断,题目难度不大,注意明确高分子化合物的特点、常见反应类型、反应原理,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
3He在月球上储量丰富,4He则来源于宇宙射线的初级粒子.下列关于3He和4He的说法正确的是( )
| A、两者互为同位素 |
| B、两者互为同素异形体 |
| C、两者为同一种原子 |
| D、两者具有相同的中子数 |
对于下列反应的说法中正确的是( )
| A、2CuFeS2+O2═Cu2S+2FeS+SO2,CuFeS2既是氧化剂又是还原剂 | ||||
| B、3NO2+H2O═2HNO3+NO氧化产物与还原产物的物质的量之比为1:2 | ||||
| C、反应KClO3+6HCl(浓)═KCl+3Cl2↑+3H2O,生成3molCl2,转移电子6mol | ||||
D、Cr2O
|
下列说法错误的( )
A、用稀硝酸洗涤试管内壁的银镜的离子方程式为:3Ag+4H++NO
| ||||||
B、浓硝酸中加入过量铁粉并加热:Fe+3NO
| ||||||
| C、过量的铜与浓硝酸反应有一氧化氮生成 | ||||||
| D、向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在试管口观察到红棕色气体 |
下列化学用语书写错误的是( )
A、原子核内有10个中子的氧原子:
| ||
| B、N2结构式:N≡N | ||
C、过氧化氢电子式: | ||
D、磷的原子结构示意图: |
下列说法不正确的是( )
| A、分散质粒子的直径在10-9~10-7m之间的分散系叫做胶体 |
| B、KAl(SO4)2在水溶液中电离方程式为KAl(SO4)2═K++Al3++SO42- |
| C、利用丁达尔效应可以鉴别CuSO4溶液和氢氧化铁胶体 |
| D、氯气可用于自来水的消毒 |
下列条件下铁钉最容易生锈的是( )
| A、浸泡在汽油中 |
| B、浸泡在盐水中 |
| C、浸泡在酒精中 |
| D、浸泡在糖水中 |
下列说法错误的( )
| A、分别充满HCl、NH3的烧瓶倒置于水中后液面迅速上升,说明二者均易溶于水 | ||||||
B、向NH4HCO3溶液中加过量的NaOH溶液并加热,离子方程式为:NH
| ||||||
| C、用NH4Cl固体和Ca(OH)2固体制备并收集NH3,需要的玻璃仪器有酒精灯、大试管、导管、集气瓶 | ||||||
| D、用湿润的红色石蕊试纸检验氨气 |
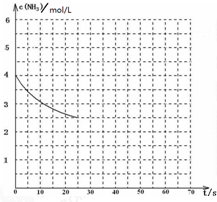 氨是最重要的化工产品之一.
氨是最重要的化工产品之一.