题目内容
合成氨反应的正反应是气体体积减小的放热反应,合成氨工业的生成流程如下:
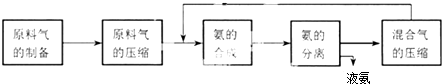
关于合成氨工业的说法中不正确的是( )

关于合成氨工业的说法中不正确的是( )
| A、混合气进行循环利用遵循绿色化学思想 |
| B、对原料气进行压缩可以增大原料气的转化率 |
| C、合成氨反应须在低温下进行 |
| D、使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动 |
考点:工业合成氨
专题:化学应用
分析:A、根据绿色化学思想:环保、无污染以及原料的利用率高来回答;
B、根据压强对化学平衡移动的影响来回答;
C、根据温度对反应速率的影响来回答;
D、催化剂的特点:提高反应的速率,但是不能使平衡移动.
B、根据压强对化学平衡移动的影响来回答;
C、根据温度对反应速率的影响来回答;
D、催化剂的特点:提高反应的速率,但是不能使平衡移动.
解答:
解:A、混合气进行循环利用可以节约能源、提高原料的利用率,这遵循绿色化学思想,故A正确;
B、对原料气进行压缩,即增大压强,化学平衡正向移动,可以增大原料气的转化率,故B正确;
C、降低温度,反应速率减慢,为保证速率较快,催化剂的活性高,产物的产率又不低,则选择适宜的温度即可,不能在低温下进行,故C错误;
D、催化剂的特点:提高反应的速率,但是不能使平衡移动,使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动,故D正确.
故选C.
B、对原料气进行压缩,即增大压强,化学平衡正向移动,可以增大原料气的转化率,故B正确;
C、降低温度,反应速率减慢,为保证速率较快,催化剂的活性高,产物的产率又不低,则选择适宜的温度即可,不能在低温下进行,故C错误;
D、催化剂的特点:提高反应的速率,但是不能使平衡移动,使用催化剂可以提高反应的速率,但是不能使平衡向正反应方向移动,故D正确.
故选C.
点评:本题涉及催化剂的特点以及化学平衡移动原理知识,注意实际和理论的应用是关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 如图:A处通入氯气.关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色.由此作出的判断正确的是( )
如图:A处通入氯气.关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色.由此作出的判断正确的是( )| A、D中可能是浓硫酸 |
| B、通入的氯气含有水蒸气 |
| C、D中可能是水 |
| D、D中不可能是NaOH溶液 |
除去乙烷中混有的少量乙烯,应采用的简便方法是( )
| A、将混合气体通过氢氧化钠溶液 |
| B、将混合气体通过溴水 |
| C、将混合气体在催化剂条件下跟氢气反应 |
| D、使混合气体中的乙烯气体发生加聚反应 |
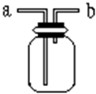 如图所示是中学化学实验中常见的装置,它有多种用途.
如图所示是中学化学实验中常见的装置,它有多种用途.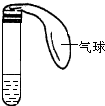 某学生课外活动小组利用如图所示装置分别做如下实验:在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是
某学生课外活动小组利用如图所示装置分别做如下实验:在试管中注入某无色溶液,加热试管,溶液变为红色,冷却后恢复无色,则此溶液可能是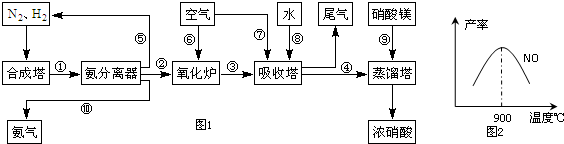
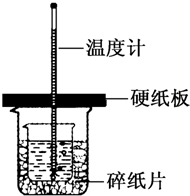 根据中和热的测定实验填空.
根据中和热的测定实验填空.