题目内容
含有Ca2+、Mg2+的溶液,在pH=10时,用EDTA标准溶液滴定,测定的是( )
| A、Ca2+、Mg2+的总含量 |
| B、Ca2+的含量 |
| C、Mg2+的含量 |
考点:常见离子的检验方法
专题:离子反应专题
分析:Mg2+开始沉淀时的pH为10,沉淀完全时的pH为11.2,Ca2+开始沉淀时的pH为12;在pH=10时,用EDTA标准溶液滴定,镁离子转化为沉淀,以此来解答.
解答:
解:溶液调节pH=10,用EDTA标准溶液滴定,镁离子全部沉淀,若加入2滴K-B指示剂,继续以某浓度的EDTA标准溶液滴定至终点,可确定钙离子和EDTA标准溶液反应消耗的溶液体积,然后可分别计算含量,
故选C.
故选C.
点评:本题考查常见离子的检验,为高频考点,把握用EDTA标准溶液滴定时沉淀的pH为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质鉴别的方法正确的是( )
| A、用焰色反应鉴别氯化钠固体和氢氧化钠固体 |
| B、用丁达尔效应鉴别NaCl溶液和KCl溶液 |
| C、用AgNO3溶液鉴别NaCl溶液和Na2SO4溶液 |
| D、用萃取法鉴别溴水和碘水 |
下列各离子浓度的大小比较,正确的是( )
| A、同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl④NH3?H2O,C(NH4+)由大到小的顺序是:①>③>②>④ |
| B、常温时,将等体积的盐酸和氨水混合后,pH=7,则C(NH4+)>C (Cl-) |
| C、0.2 mol/LNa2CO3溶液中:C (OH-)=C (HCO3-)+C (H+)+C (H2CO3) |
| D、同浓度的下列溶液中,①NaCl ②Na2CO3 ③CH3COONa④NaOH,pH值由大到小的顺序是:④>③>②>① |
埋在地下的输油铸铁管道,在下列各种情况下,腐蚀速度最快的是( )
| A、在潮湿的酸性土壤中 |
| B、在潮湿不透气的中性土壤中 |
| C、在干燥致密不透气的土壤中 |
| D、在潮湿透气的盐碱地中 |
下列各组离子一定可以大量共存的是( )
| A、在含大量Al3+的溶液中:NH4+、Na+、HCO3-、SO42- |
| B、能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、NO3- |
| C、在水电离出的c(H+)=10-13mol?L-1 的溶液中:NH4+、[Al(OH)4]-、SO42-、NO3- |
| D、在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
下列每组中各有三种混合物,它们都能用分液漏斗分离的是( )
| A、乙酸乙酯和水,酒精和水,植物油和水 |
| B、甘油和水,乙酸和水,乙酸和乙醇 |
| C、四氯化碳和水,溴苯和水,硝基苯和水 |
| D、汽油和水,苯和水,乙醛和水 |


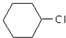 为原料合成重要的化工产品
为原料合成重要的化工产品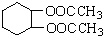 的路线流程图(无机试剂任选)合成路线流程图示例如图2.
的路线流程图(无机试剂任选)合成路线流程图示例如图2.

