题目内容
9.(1)有以下八种饱和溶液:①Ba(NO3)2;②Ca(OH)2;③Ca(ClO)2;④CaCl2;⑤Na2CO3;⑥NaAlO2;⑦NH3和NaCl;⑧Na2SiO3.向其中分别持续通入CO2,最终能得到沉淀或析出晶体的⑤⑥⑦⑧.(2)根据下列描述写出下列化学方程式:
①已知ZnO属于两性氧化物,写出ZnO与NaOH溶液反应的离子方程式:ZnO+2OH-=Zn02-+H2O.
②联氨(N2H4)是航天飞船常用的高能燃料.联氨可以采用尿素[CO(NH2)2]为原料制取,方法是在高锰酸钾催化剂存在下,尿素【CO(NH2)2】和次氯酸钠、氢氧化钠溶液反应生成联氨、碳酸钠、另一种钠盐和水,写出其反应的化学方程式:CO(NH2)2+NaClO+2NaOH$\frac{\underline{\;KMnO_{4}\;}}{\;}$N2H4+NaCl+Na2CO3+H2O.
分析 (1)①碳酸比硝酸弱,与硝酸钡不反应;
②酸性氧化物能与碱反应,过量的CO2与Ca(OH)2 反应:Ca(OH)2+2CO2═Ca(HCO3)2;
③碳酸酸性强于次氯酸,二氧化碳能与次氯酸钙反应,但通入过量CO2后无沉淀;
④碳酸比盐酸弱,CO2与CaCl2溶液不会反应;
⑤过量的CO2通入饱和Na2CO3溶液中发生反应生成碳酸氢钠;
⑥NaAlO2溶液通入过量的二氧化碳,可生成氢氧化铝沉淀;
⑦可生成碳酸氢钠和氯化铵,为侯氏制碱法原理;
⑧碳酸比硅酸强,过量的CO2与Na2SiO3溶液反应生成硅酸沉淀;
(2)ZnO为两性氧化物,与氢氧化钠溶液反应生成可溶性的锌酸盐(Zn02-)和H2O;
②高锰酸钾作催化剂,从反应物以及产物可以看出该反应为氧化还原反应,氯由+1价变为了-1价,而碳变为了+4价的碳酸根.
解答 解:(1)①碳酸比硝酸弱,二氧化碳与Ba(NO3)2溶液不反应,没有沉淀生成,故①错误;
②酸性氧化物能与碱反应,过量的CO2与Ca(OH)2 反应:Ca(OH)2+2CO2═Ca(HCO3)2,无沉淀生成,故②错误;
③次氯酸是比碳酸还弱的酸,所以二氧化碳、水和次氯酸钙反应生成碳酸钙沉淀,但二氧化碳是过量的,过量的二氧化碳和碳酸钙能继续反应生成可溶性的碳酸氢钙,所以最终没有沉淀析出,故③错误;
④碳酸比盐酸弱,CO2与CaCl2溶液不会反应,无沉淀生成,故④错误;
⑤过量的CO2通入饱和Na2CO3溶液中发生反应:Na2CO3+H2O+CO2═2NaHCO3↓,因为碳酸氢钠溶解度比碳酸钠小,所以有NaHCO3晶体析出,故⑤正确;
⑥NaAlO2溶液通入过量的二氧化碳,由于碳酸酸性比氢氧化铝强,所以生成氢氧化铝白色沉淀和碳酸氢钠,2H2O+NaAlO2+CO2=Al(OH)3↓+NaHCO3,故⑥正确;
⑦反应发生NH3+CO2+NaCl+H2O=NaHCO3↓+NH4Cl,所以有NaHCO3晶体析出,故⑦正确;
⑧碳酸比硅酸强,过量的CO2与Na2SiO3溶液反应:2CO2+Na2SiO3+2H2O═2NaHCO3+H2SiO3↓,产生硅酸沉淀,故③正确;
故答案为:⑤⑥⑦⑧;
(2)①已知ZnO为两性氧化物,与氢氧化钠溶液反应生成可溶性的锌酸盐(Zn02-),离子方程式为ZnO+2OH-=Zn02-+H2O,
故答案为:ZnO+2OH-=Zn02-+H2O;
②高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种盐和水,该反应发生了氧化还原反应,氯由+1价变为了-1价,即ClO-变为了Cl-,而尿素变为+4价的碳酸根,其反应方程式为CO(NH2)2+NaClO+2NaOH$\frac{\underline{\;KMnO_{4}\;}}{\;}$N2H4+NaCl+Na2CO3+H2O,
故答案为:CO(NH2)2+NaClO+2NaOH$\frac{\underline{\;KMnO_{4}\;}}{\;}$N2H4+NaCl+Na2CO3+H2O.
点评 本题考查了元素及其化合物的性质,为高考常见题型,侧重于元素化合物知识的综合理解和运用的考查,注意基础知识的掌握,题目难度中等.

| A. | 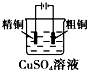 铜的冶炼 | B. | 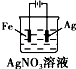 铁上镀银 | C. | 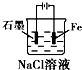 防止Fe被腐蚀 | D. | 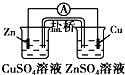 构成铜锌原电池 |
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸 | |
| C. | 酒精灯着火时可用沙子扑灭 | |
| D. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 |
| A. | Q一定是氧化剂 | |
| B. | 当有1 mol O2生成时转移电子4 mol | |
| C. | O2一定是氧化产物 | |
| D. | Na2O2不可能发生还原反应 |




 .
.