题目内容
【题目】甲醇是一种重要的化工原料,有着重要的用途和应用前景. 甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.
某实验小组设计了如图所示的甲醇燃料电池装置.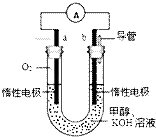
①该电池工作时,通入氧气的电极名称为 , 电极反应式为 . 另一电极反应式为 . 氢氧根离子流向极(填正或负)
②工作一段时间后,测得溶液的碱性(填增强或减弱).
【答案】正极;O2+2H2O+4e﹣=4OH﹣;CH3OH+8OH﹣﹣6e﹣=CO32﹣+6H2O;负;减弱
【解析】解:①燃料电池的工作原理:通入甲醇的一极为负极,负极上甲醇失电子生成碳酸根离子,则负极的电极反应式为:CH3OH+8OH﹣﹣6e﹣=CO32﹣+6H2O,通入氧气的一极为正极,正极上氧气得电子生成氢氧根离子,正极的电极反应式为:O2+2H2O+4e﹣=4OH﹣;电解质溶液中氢氧根离子向负极移动; 所以答案是:正极;O2+2H2O+4e﹣=4OH﹣;CH3OH+8OH﹣﹣6e﹣=CO32﹣+6H2O;负;②在碱性环境下,甲醇反应生成的二氧化碳会消耗氢氧根离子,所以溶液的碱性减弱;所以答案是:减弱.

练习册系列答案
相关题目