题目内容
9.设NA为阿伏加徳罗常数的值,下列说法正确的是( )| A. | 糖类、油脂、蛋白质都能发生水解反应,但水解产物不同 | |
| B. | 25℃、lOlkPa时,2.24LCH4含有的共价键数为0.4NA | |
| C. | 56g聚乙烯中含有碳碳双键的数目为2键 | |
| D. | 2.8g硅单质与足量氧气在高温下完全反应时,硅原子失去的电子数目为0.4NA |
分析 A、糖分为单糖、二糖和多糖;
B、25℃101Kp时,气体摩尔体积大于22.4L/mol;
C、聚乙烯是乙烯的加聚产物;
D、求出硅的物质的量,然后根据硅和氧气反应后变为+4价来分析.
解答 解:A、糖分为单糖、二糖和多糖,而单糖不能水解,故A错误;
B、25℃101Kp时,气体摩尔体积大于22.4L/mol,故2.24L甲烷的物质的量小于0.1mol,故含有的共价键个数小于0.4NA个,故B错误;
C、聚乙烯是乙烯的加聚产物,故聚乙烯中无碳碳双键,故C错误;
D、2.8g硅的物质的量为0.1mol,而硅和氧气反应后变为+4价,故0.1mol硅和氧气反应后失去0.4NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列变化中,属于物理变化的是( )
| A. | 从石油中分馏出汽油 | B. | 煤的气化制水煤气 | ||
| C. | 煤的干馏制焦炭 | D. | 油脂的水解制肥皂 |
20.只含镁、镍和碳三种元素的新型超导晶体的一个晶胞如图所示,则该晶体的化学式为( )
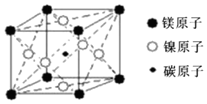

| A. | MgCNi3 | B. | MgC2Ni | C. | MgCNi2 | D. | Mg2CNi3 |
17.在一定条件下发生反应:2A(g)+2B(g)?xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率v(D)=0.2mol•L-1•min-1,下列说法正确的是( )
| A. | A和B的转化率均是20% | B. | x=2 | ||
| C. | 平衡时B的物质的量为1.2mol | D. | 平衡时气体压强比原来减小 |
14.有关煤的综合利用如图所示.下列说法正确的是( )


| A. | ①是将煤在空气中加强热使其分解的过程 | |
| B. | 煤中含有苯、甲苯、二甲笨等有机物 | |
| C. | ②是放热的过程 | |
| D. | B为甲醇或乙酸时,原子利用率均达到100% |
1.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1NaAlO2溶液:H+、Na+、Cl-、SO42- | |
| B. | 使甲基橙变黄的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42- | |
| C. | 水电离的H+浓度为10-12mol•L-1的溶液中:Cl-、CO32-、NO3-、SO32- | |
| D. | pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32- |
1.常温下,经测定某溶液中离子只有Na+、CH3COO-、H+、OH-四种,且四种离子浓度大小的排列顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-),其可能的情形是( )
①该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成;
②该溶液由0.2mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成;
③该溶液由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成;
④该溶液为0.1mol/L的CH3COONa溶液.
①该溶液由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成;
②该溶液由0.2mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成;
③该溶液由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成;
④该溶液为0.1mol/L的CH3COONa溶液.
| A. | ①④ | B. | ②③ | ||
| C. | ①② | D. | ③④ | ||
| E. | 故①②可能,答案选C. |
2.下列事实可以用氢键解释的是( )
| A. | I2易溶于CCl4,难溶于水 | B. | 水结成冰体积膨胀,密度变小 | ||
| C. | CH4、C2H6、C3H8的熔、沸点依次升高 | D. | HCl、HBr、HI的热稳定性依次减弱 |
