题目内容
下列离子在溶液中能大量存在的( )
| A、K+、MnO4-、Cl-、H+ |
| B、AlO2-、Na+、Al3+、Cl- |
| C、Fe2+、SO42-、Cl-、Na+ |
| D、H+、AlO2-、Na+、Cl- |
考点:离子共存问题
专题:离子反应专题
分析:如离子之间不发生复分解反应生成沉淀、气体或水,或不发生氧化还原反应、互促水解等反应,则可大量共存,反之不能,以此解答该题.
解答:
解:A.酸性条件下,MnO4-、Cl-发生氧化还原反应,不能大量共存,故A错误;
B.AlO2-与Al3+发生互促水解反应生成沉淀而不能大量共存,故B错误;
C.离子之间不发生任何反应,可大量共存,故C正确;
D.H+、AlO2-反应生成氢氧化铝或铝离子而不能大量共存,故D错误.
故选C.
B.AlO2-与Al3+发生互促水解反应生成沉淀而不能大量共存,故B错误;
C.离子之间不发生任何反应,可大量共存,故C正确;
D.H+、AlO2-反应生成氢氧化铝或铝离子而不能大量共存,故D错误.
故选C.
点评:本题考查离子共存,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握离子的性质以及反应类型的判断,难度不大.

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目
用98%的浓H2SO4(密度为1.84g/cm3)配制1mol/L的稀H2SO4 90mL,配制过程中需用仪器的先后顺序是( )
①20mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒.
①20mL量筒 ②10mL量筒 ③50mL烧杯 ④托盘天平 ⑤100mL容量瓶 ⑥胶头滴管 ⑦玻璃棒.
| A、①③⑤⑥⑦ |
| B、②③⑦⑤⑥ |
| C、②⑤⑦⑥① |
| D、④③⑦⑤⑥ |
某固体混合物含有等物质的量且均为1mol的CuSO4、KCl、NaOH、NH4Cl四种成分中的某两种.通过实验确定其组成:取少量固体溶于水,得到无色澄清的溶液;向该溶液中滴入少量的硝酸铝溶液,看到有白色沉淀生成.该固体混合物的组成是( )
| A、NaOH、NH4Cl |
| B、KCl、CuSO4 |
| C、KCl、NaOH |
| D、KCl、NH4Cl |
固体粉末X中可能含有Fe、Fe2O3、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3中的若干种.为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如下:根据上述实验,以下说法正确的是( )
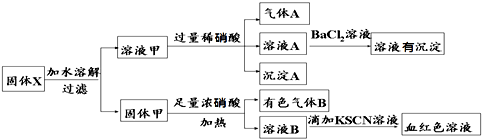

| A、气体A一定只是NO |
| B、由于在溶液A中加入BaCl2溶液有沉淀产生,因此可以判断溶液中含有K2SO3 |
| C、若向固体甲中加入足量浓盐酸,再加KSCN溶液,没有血红色,则证明原混合物中一定没有Fe2O3 |
| D、溶液甲中一定含有K2SiO3、可能含有KAlO2、MgCl2 |
下列实验装置图所示的实验操作,能达到相应的实验目的是( )
A、 分离沸点相差较大液体混合物 |
B、 除去CO气体中的CO2气体 |
C、 向容量瓶中转移液体 |
D、 分离互不相溶的两种液体 |
下列哪项做法,不能有助于能源“开源节流”( )
| A、大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源 |
| B、减少资源消耗,增加资源的重复利用、资源的循环再生 |
| C、发展低碳经济,推广利用电能、风能的城市照明系统 |
| D、大力开采煤、石油和天然气以满足人们日益增长的能源需求 |