题目内容
A、B、C、D分别为(NH4)2SO4、Ba(OH)2、AlCl3、Na2CO3 4种物质中的1种,现进行如下实验:
①实验测得A溶液和D溶液显碱性,B溶液和C溶液显酸性;
②A溶液和D溶液混合可生成沉淀甲
③足量A溶液与B溶液混合共热可生成沉淀乙和刺激性气味气体;
请回答:
(1)B的化学式为 ;沉淀甲的化学式为 .
(2)足量A溶液与B溶液混合共热生成沉淀乙和刺激性气味气体的离子方程式为 .
(3)加热蒸干C溶液并灼烧,最后所得固体为 (填化学式).
(4)D溶液中各离子浓度由大到小的顺序为 .
(5)已知25℃时沉淀甲的Ksp=5.1×10-9 mol2?L-2,沉淀乙的Ksp=1.1×10-10 mol2?L-2.将沉淀甲加入到B溶液中,沉淀甲会转化为沉淀乙.写出该转化反应的离子方程式: .
①实验测得A溶液和D溶液显碱性,B溶液和C溶液显酸性;
②A溶液和D溶液混合可生成沉淀甲
③足量A溶液与B溶液混合共热可生成沉淀乙和刺激性气味气体;
请回答:
(1)B的化学式为
(2)足量A溶液与B溶液混合共热生成沉淀乙和刺激性气味气体的离子方程式为
(3)加热蒸干C溶液并灼烧,最后所得固体为
(4)D溶液中各离子浓度由大到小的顺序为
(5)已知25℃时沉淀甲的Ksp=5.1×10-9 mol2?L-2,沉淀乙的Ksp=1.1×10-10 mol2?L-2.将沉淀甲加入到B溶液中,沉淀甲会转化为沉淀乙.写出该转化反应的离子方程式:
考点:无机物的推断
专题:
分析:A、B、C、D分别为(NH4)2SO4、Ba(OH)2、AlCl3、Na2CO3 4种物质中的1种,实验测得A溶液和D溶液显碱性,则A、D为Ba(OH)2、Na2CO3,B溶液和C溶液显酸性,则B、C为(NH4)2SO4、AlCl3;足量A溶液与B溶液混合共热可生成沉淀乙和刺激性气味气体,则A、B为Ba(OH)2、(NH4)2SO4,沉淀乙为BaSO4,刺激性气味气体为氨气;A溶液和D溶液混合可生成沉淀甲,则A、D为Ba(OH)2、Na2CO3,沉淀甲为BaCO3,综合上述分析可知,A为Ba(OH)2,B为(NH4)2SO4,C为AlCl3,D为Na2CO3,据此答题.
解答:
解:A、B、C、D分别为(NH4)2SO4、Ba(OH)2、AlCl3、Na2CO3 4种物质中的1种,实验测得A溶液和D溶液显碱性,则A、D为Ba(OH)2、Na2CO3,B溶液和C溶液显酸性,则B、C为(NH4)2SO4、AlCl3;足量A溶液与B溶液混合共热可生成沉淀乙和刺激性气味气体,则A、B为Ba(OH)2、(NH4)2SO4,沉淀乙为BaSO4,刺激性气味气体为氨气;A溶液和D溶液混合可生成沉淀甲,则A、D为Ba(OH)2、Na2CO3,沉淀甲为BaCO3,综合上述分析可知,A为Ba(OH)2,B为(NH4)2SO4,C为AlCl3,D为Na2CO3,
(1)根据上面的分析可知,B的化学式为(NH4)2SO4;沉淀甲的化学式为BaCO3,
故答案为:(NH4)2SO4;BaCO3;
(2)足量A溶液与B溶液混合共热生成沉淀乙和刺激性气味气体的离子方程式为2NH4++SO42-+Ba2++2OH-=BaSO4↓+2NH3↑+2H2O,
故答案为:2NH4++SO42-+Ba2++2OH-=BaSO4↓+2NH3↑+2H2O;
(3)C为AlCl3,铝离子会发生水解,生成氢氧化铝,氢氧化铝受热分解得氧化铝,所以加热蒸干C溶液并灼烧,最后所得固体为Al2O3,
故答案为:Al2O3;
(4)D为Na2CO3,碳酸根离子发生水解,溶液呈碱性,所以D溶液中各离子浓度由大到小的顺序为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),
故答案为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+);
(5)已知25℃时沉淀甲的Ksp=5.1×10-9 mol2?L-2,沉淀乙的Ksp=1.1×10-10 mol2?L-2.将沉淀甲加入到B溶液中,沉淀甲会转化为沉淀乙,该转化反应的离子方程式为:BaCO3(s)+SO42-(aq)=BaSO4(s)+CO3 2-(aq),
故答案为:BaCO3(s)+SO42-(aq)=BaSO4(s)+CO3 2-(aq);
(1)根据上面的分析可知,B的化学式为(NH4)2SO4;沉淀甲的化学式为BaCO3,
故答案为:(NH4)2SO4;BaCO3;
(2)足量A溶液与B溶液混合共热生成沉淀乙和刺激性气味气体的离子方程式为2NH4++SO42-+Ba2++2OH-=BaSO4↓+2NH3↑+2H2O,
故答案为:2NH4++SO42-+Ba2++2OH-=BaSO4↓+2NH3↑+2H2O;
(3)C为AlCl3,铝离子会发生水解,生成氢氧化铝,氢氧化铝受热分解得氧化铝,所以加热蒸干C溶液并灼烧,最后所得固体为Al2O3,
故答案为:Al2O3;
(4)D为Na2CO3,碳酸根离子发生水解,溶液呈碱性,所以D溶液中各离子浓度由大到小的顺序为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+),
故答案为:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+);
(5)已知25℃时沉淀甲的Ksp=5.1×10-9 mol2?L-2,沉淀乙的Ksp=1.1×10-10 mol2?L-2.将沉淀甲加入到B溶液中,沉淀甲会转化为沉淀乙,该转化反应的离子方程式为:BaCO3(s)+SO42-(aq)=BaSO4(s)+CO3 2-(aq),
故答案为:BaCO3(s)+SO42-(aq)=BaSO4(s)+CO3 2-(aq);
点评:本题考查无机物的推断,利用物质反应的现象推断各物质为解答的关键,有一定的综合性,题目难度中等,答题时注意常见元素化合物知识的应用.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
 某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子.当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化的如图所示,下列说法正确的是( )
某溶液中可能含有OH-、CO32-、AlO2-、SiO32-、SO42-、Na+、Fe3+、Mg2+、Al3+等离子.当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀物质的量随盐酸的体积变化的如图所示,下列说法正确的是( )| A、原溶液一定含有Na2SO4 |
| B、反应最后形成的溶液中的溶质为NaCl |
| C、原溶液中一定含有的阴离子是OH-、CO32-、AlO2-、SO42- |
| D、原溶液中含有CO32- 与AlO2-的物质的量之比为3:4 |
下列反应进行分类时,既属于氧化还原反应又属于化合反应的是( )
| A、CO2+H2O═H2CO3 |
| B、2KClO3═2KCl+3O2↑ |
| C、S+O2═SO2 |
| D、CH4+2O2═CO2+2H2O |
绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是( )
A、甲烷与氯气反应制氯仿:CH4+3Cl2
| ||
B、烯烃与水煤气发生的羰基合成反应:RCH=CH2+CO+H2
| ||
C、甲烷、CO合成乙酸乙酯:2CH4+2CO
| ||
D、乙烯合成聚乙烯nCH2-CH2
 |
下列有关离子浓度的关系不正确的是( )
| A、pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) |
| B、若常温下,0.1mol/L的二元酸H2A溶液c(H+)=0.11mol/L,则Na2A稀溶液中:c(Na+)=2c(A2-)+2c(HA-)+2c(H2A) |
| C、NaHCO3与NaHSO3混合反应的中性溶液中:c(Na+)=c(HSO3-)+2c(SO32-)+c(HCO3-)+2c(CO32-) |
| D、浓度均为0.1mol/L的CH3COOH与CH3COONa溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
下列颜色不属于因化学反应而产生的现象的是( )
| A、双氧水使品红溶液褪色 |
| B、久置的KI溶液呈黄色 |
| C、新制氯水久置后变为无色 |
| D、普通玻璃导管口点燃纯净氢气时,火焰呈黄色 |

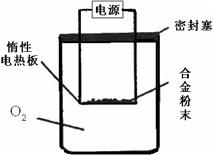 锌和铝都是活泼金属,化学性质相似,其氢氧化物既能溶于强酸,也能溶于强碱,都是两性氢氧化物.但是氢氧化铝不溶于氨水,而氢氧化锌却溶于氨水生成[Zn(NH3)4]2+,回答下列问题:
锌和铝都是活泼金属,化学性质相似,其氢氧化物既能溶于强酸,也能溶于强碱,都是两性氢氧化物.但是氢氧化铝不溶于氨水,而氢氧化锌却溶于氨水生成[Zn(NH3)4]2+,回答下列问题: