题目内容
某温度下1 L密闭容器中加1 mol N2和3 mol H2,使反应N2+3H2![]() 2NH3达到平衡,测得平衡混合气体中N2、H2,NH3物质的量分别为m mol,n mol,q mol.如温度不变,只改变初始加入的物质的量,而要求m、n、q的值维持不变,则N2,H2,NH3加入的物质的量用x、y、z表示时,应满足条件:
2NH3达到平衡,测得平衡混合气体中N2、H2,NH3物质的量分别为m mol,n mol,q mol.如温度不变,只改变初始加入的物质的量,而要求m、n、q的值维持不变,则N2,H2,NH3加入的物质的量用x、y、z表示时,应满足条件:
(1)若x=0,y=0,则z=________.
(2)若x=0.75 mol,则y=________,q=________
(3)x、y、z应满足的一般条件是(请用两上方程式表示,其中一个含x和y,另一个只含y和z)________.
答案:
解析:
解析:
|
(1)2 mol (2)2.25 mol,0.5 mol (3)y=3x 3z+2y=6 |

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
 已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:
已知,某温度下在2L密闭容器中加入一定量A,发生以下化学反应:2A(g)═B(g)+C(g);△H=-48.25kJ?mol-1
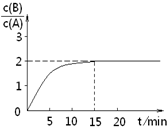
反应过程中时间t与A、B浓度有如图关系,若测得第15min时
c(B)=1.6mol?L-1,则下列结论正确的是( )
| A、反应在前15min的平均速率ν(A)=0.11 mol?L-1?min-1 | B、A的初始物质的量为8 mol | C、反应到达平衡的过程中,放出的热量是77.2kJ | D、如使反应最终c(B)/c(A)=1.5,恒温恒容时,加入一定量的A可以实现 |
 能源短缺是人类面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.