题目内容
下列实验装置设计正确的是( )
A、 实验室制氢气 |
B、 稀释浓硫酸 |
C、 NaOH溶液吸收HCl气体 |
D、 分离碘酒中的碘和酒精 |
考点:化学实验方案的评价,物质的分离、提纯的基本方法选择与应用,尾气处理装置,常见气体制备原理及装置选择
专题:实验评价题
分析:A.可用简易气体发生装置制备氢气;
B.稀释浓硫酸,应防止酸液飞溅;
C.进气管应贴近液面;
D.碘易溶于酒精,用分液的方法不能分离.
B.稀释浓硫酸,应防止酸液飞溅;
C.进气管应贴近液面;
D.碘易溶于酒精,用分液的方法不能分离.
解答:
解:A.实验室用稀硫酸和锌粒反应制备氢气,可用简易气体发生装置制备,故A正确;
B.浓硫酸溶于水放出大量的热,易导致酸液飞溅,应将浓硫酸沿烧杯内壁缓缓注入盛有水的烧杯中,并用玻璃棒不断搅拌,故B错误;
C.进气管应贴近液面,否则不能吸收HCl,故C错误;
D.碘易溶于酒精,用分液的方法不能分离,应用蒸馏的方法,故D错误.
故选A.
B.浓硫酸溶于水放出大量的热,易导致酸液飞溅,应将浓硫酸沿烧杯内壁缓缓注入盛有水的烧杯中,并用玻璃棒不断搅拌,故B错误;
C.进气管应贴近液面,否则不能吸收HCl,故C错误;
D.碘易溶于酒精,用分液的方法不能分离,应用蒸馏的方法,故D错误.
故选A.
点评:本题考查较为综合,涉及气体的制备、溶液的稀释、气体的收集以及物质的分离等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关基本实验操作的注意事项,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
下列关于化学反应速率的说法中正确的是( )
| A、决定化学反应速率的主要因素是温度 |
| B、反应速率用于衡量化学反应进行快慢 |
| C、可逆反应达到平衡状态时正逆反应的速率都为0 |
| D、增大反应物的量或提高反应温度一定能增大反应速率 |
下列化学用语书写正确的是( )
A、CH4分子的比例模型: |
B、氯原子的结构示意图: |
C、NH3分子的电子式: |
| D、CS2结构式:S=C=S |
常温下,0.2mol?L-1的盐酸30mL分别与下列Na2CO3溶液混合,再加水稀释到100mL,其中最初产生CO2的速率最快的是( )
| A、20mL 0.3mol?L-1 Na2CO3 |
| B、10mL 0.4mol?L-1 Na2CO3 |
| C、25mL 0.4mol?L-1 Na2CO3 |
| D、15mL 0.5mol?L-1 Na2CO3 |
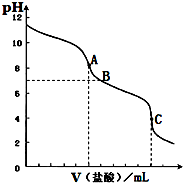 用0.1000mol?L-1的盐酸滴定10.00mL 0.1000mol?L-1的碳酸钠溶液,溶液pH值与加入盐酸的体积的关系如图所示.已知室温时饱和CO2的pH为3.9,0.05mol?L-1 NaHCO3的pH约为8.3.下列叙述中不正确的是( )
用0.1000mol?L-1的盐酸滴定10.00mL 0.1000mol?L-1的碳酸钠溶液,溶液pH值与加入盐酸的体积的关系如图所示.已知室温时饱和CO2的pH为3.9,0.05mol?L-1 NaHCO3的pH约为8.3.下列叙述中不正确的是( )| A、以酚酞为指示剂,溶液颜色突变时(A点),Na2CO3转化为NaHCO3 |
| B、以甲基橙为指示剂,当溶液颜色突变时,共消耗盐酸20.00mL |
| C、溶液pH=7时(B点),Na2CO3完全转化为NaCl |
| D、BC段对应溶液中CO2与NaHCO3共存 |
下列关于实验原理及操作的说法正确的是( )
| A、用盐析法分离氯化钠溶液和淀粉胶体 |
| B、乙醇脱水制备乙烯的实验中,可选用浓硫酸或P2O5作反应的催化剂 |
| C、味精是常见的家用调味品,其主要成分是谷氨酸钠.谷氨酸是一种氨基酸,与双缩脲试剂呈现紫玫瑰色 |
| D、用碱式滴定管量取一定量的氢氧化钠溶液,需先用该NaOH溶液润洗3次,然后加入NaOH溶液,排除橡皮管中的气泡后,注意调节液面需位于“0”刻度 |
下列说法不正确的是( )
| A、将水杨酸、乙酸酐和浓硫酸在锥形瓶中混合后,85-90℃水浴加热5-10min,取出锥形瓶,置于冰水浴中,使阿司匹林结晶析出,为了使其结晶完全需要向锥形瓶中继续加适量的水 |
| B、用移液管取液后,将移液管稍倾斜放入锥形瓶中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
| C、相同条件下,10mL 0.1mol/L FeCl2溶液中滴入1mL 0.1mol/L NaNO2溶液,溶液颜色由浅绿色变成黄色,10mL 0.1mol/L KI溶液中滴入1mL 0.1mol/L NaNO2溶液,溶液颜色无变化,说明溶液的pH会影响NO2-的氧化性 |
| D、为了检验火柴头中的硫元素,先用刀片削下几根火柴的火柴头,放入一支中号试管中,先用酒精灯加热该试管底部引燃“火药”,然后塞上橡皮塞待用 |
某反应过程能量变化如图所示,下列说法正确的是( )


| A、反应过程a有催化剂参与 |
| B、该反应为放热反应,热效应等于△H |
| C、改变催化剂,可改变该反应的活化能 |
| D、在催化剂条件下,反应的活化能等于E1+E2 |
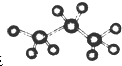
 与C8H6互为同分异构体.
与C8H6互为同分异构体.