题目内容
完成物质的量的相关计算
(1)0.5mol H2SO4 的质量是 g,含 个氧原子,能和 mol NaOH完全反应.
(2)标准状况下100mL某气体的质量是0.125g,该气体的相对分子质量为 .
(3)将标准状况下2240mL HCl气体溶于水配成100mL溶液,则所得盐酸的物质的量浓度为 ,若所得溶液密度为1g/mL,则该盐酸的质量分数为 .
(1)0.5mol H2SO4 的质量是
(2)标准状况下100mL某气体的质量是0.125g,该气体的相对分子质量为
(3)将标准状况下2240mL HCl气体溶于水配成100mL溶液,则所得盐酸的物质的量浓度为
考点:物质的量的相关计算
专题:计算题
分析:结合n=
=
=cV以及相关反应的方程式计算.
| m |
| M |
| N |
| NA |
解答:
解:(1)m(H2SO4)=0.5mol×98g/mol=49g,N(O)=0.5mol×4×NA/mol=2NA,
由方程式H2SO4+2NaOH=Na2SO4+2H2O可知,需要1molNaOH,
故答案为:49;2NA;1;
(2)n=
,则M=
=
=28g/mol,则该气体的相对分子质量为28,故答案为:28;
(3)n(HCl)=
=0.1mol,
c(HCl)=
=1mol/L,
ω(HCl)=
×100%=3.65%,
故答案为:1mol/L; 3.65%.
由方程式H2SO4+2NaOH=Na2SO4+2H2O可知,需要1molNaOH,
故答案为:49;2NA;1;
(2)n=
| 0.1L |
| 22.4L/mol |
| m |
| n |
| 0.125g | ||
|
(3)n(HCl)=
| 2.24L |
| 22.4L/mol |
c(HCl)=
| 0.1mol |
| 0.1L |
ω(HCl)=
| 0.1mol×36.5g/mol |
| 100mL×1g/mL |
故答案为:1mol/L; 3.65%.
点评:本题考查物质的量的相关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,难度不大,注意相关计算公式、单位以及概念的理解和运用.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
下列说法中正确的是( )
| A、元素的存在形态有两种:化合态和游离态 |
| B、有多少种元素就有多少种物质 |
| C、同一元素呈化合态时,其化合价一定比游离态时高 |
| D、同一元素在不同的物质中的价态一定不同 |
用铜锌合金制成假金元宝骗人的事件屡有发生,下列不可以区别其真伪的方法是( )
| A、测定密度 | B、放入硝酸中 |
| C、放入盐酸中 | D、观察外观 |
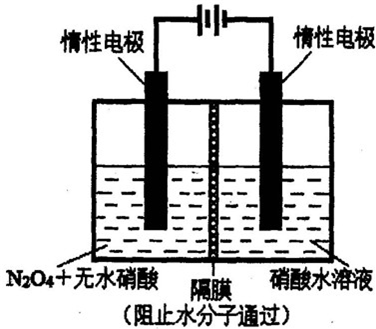 N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
N2O5是一种新型硝化剂,其性质和制备受到人们的关注.