题目内容
【题目】设![]() 表示阿伏加德罗常数的值,下列说法中正确的
表示阿伏加德罗常数的值,下列说法中正确的
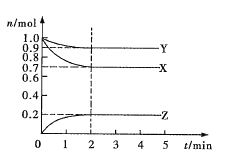
![]() 一定条件下定容容器中充入
一定条件下定容容器中充入![]() 和
和![]() 发生反应:3
发生反应:3![]() ;
;![]() ,当该反应放出
,当该反应放出![]() 的热量时,容器中的氢分子数共有
的热量时,容器中的氢分子数共有![]()
![]() 常温下,
常温下,![]() 和
和![]() 的混合物中含有的碳原子数为
的混合物中含有的碳原子数为![]()
![]() 硫酸钠固体中含有
硫酸钠固体中含有![]() 个硫酸钠分子;
个硫酸钠分子;
![]() 中含有的质子数、中子数、电子数均为
中含有的质子数、中子数、电子数均为![]()
![]() 标准状况下,
标准状况下,![]() 氯仿中含有
氯仿中含有![]() 键的数目为
键的数目为![]()
![]() 将
将![]() 的
的![]() 溶液滴入沸水中可制得
溶液滴入沸水中可制得![]() 胶粒
胶粒![]() .
.
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】C
【解析】
![]() 依据热化学方程式的定量关系计算分析,反应焓变是指对应化学方程式物质全部反应时放出的热量,一定条件下定容容器中充入
依据热化学方程式的定量关系计算分析,反应焓变是指对应化学方程式物质全部反应时放出的热量,一定条件下定容容器中充入![]() 和
和![]() 发生反应:
发生反应:![]() ;
;![]() ,当该反应放出
,当该反应放出![]() 的热量时,容器中的氢分子数=(3mol-0.75mol)NA mol-1=2.25NA,故
的热量时,容器中的氢分子数=(3mol-0.75mol)NA mol-1=2.25NA,故![]() 正确;
正确;
![]() 和
和![]() 的最简比为
的最简比为![]() ,
,![]() 中碳原子数=
中碳原子数=![]() ×NA mol-1=1.5NA,故
×NA mol-1=1.5NA,故![]() 正确;
正确;
![]() 硫酸钠是离子化合物不存在分子,故
硫酸钠是离子化合物不存在分子,故![]() 错误;
错误;
![]() 依据
依据![]() 计算物质的量
计算物质的量![]() ,结合分子式计算含有的质子数
,结合分子式计算含有的质子数![]() 、中子数
、中子数![]() 、电子数为
、电子数为![]() ,故
,故![]() 正确;
正确;
![]() 氯仿标准状况不是气体,
氯仿标准状况不是气体,![]() 氯仿物质的量不是
氯仿物质的量不是![]() ,故
,故![]() 错误;
错误;
![]() 胶体微粒是氢氧化铁的集合体,将
胶体微粒是氢氧化铁的集合体,将![]() 的
的![]() 溶液滴入沸水中可制得
溶液滴入沸水中可制得![]() 胶粒小于
胶粒小于![]() 故
故![]() 错误;
错误;
故选C。

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案【题目】下列实验操作或装置符合实验要求的是()
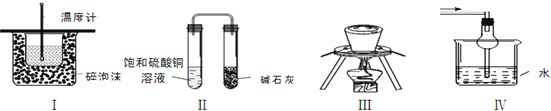
A.装置Ⅰ可用于测定中和热
B.装置Ⅱ装置放置一段时间后,饱和![]() 溶液中不出现蓝色晶体
溶液中不出现蓝色晶体
C.装置Ⅲ中的石英坩埚可用于熔化氢氧化钠
D.装置Ⅳ可用于吸收易溶于水的尾气
【题目】在某温度下,向三个初始体积为1L的密闭容器中按表所示投料,发生反应N2(g)+3H2(g)2NH3(g)△H<0,达到平衡时,下列说法错误的是
容器编号 | 容器类型 | 起始物质的量 | 反应物的转化率 | 平时时 | ||
|
|
| ||||
Ⅰ | 恒温恒容 | 1 | 3 | 0 |
|
|
Ⅱ | 绝热恒容 | 0 | 0 | 2 |
| a |
Ⅱ | 恒温恒压 | 1 | 3 | 0 |
| b |
A.平衡时NH3的物质的量:a>1.2,b>1.2
B.容器I、II中平衡常数关系:K(I)>K(II)
C.a1+a2<1
D.若起始时向容器A中充入lmolN2(g)、0.4molH2(g)、0.4molNH3(g),此时平衡向正反应方向移动