题目内容
欲同时对农作物施用含N、P、K三种元素的化肥,现有:①K2CO3、②KCl、③Ca(H2PO4)2、④(NH4)2SO4、⑤氨水,最适合的组合是( )。
| A.①②③ | B.②③④ | C.①③⑤ | D.②③⑤ |
B
解析

练习册系列答案
相关题目
下列能正确表示水解的离子方程式是
A.CH3COOH + H2O 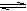 CH3COO- + H3O+ CH3COO- + H3O+ |
B.NH4+ + H2O 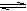 NH3·H2O + H+ NH3·H2O + H+ |
C.CO32- + 2H2O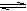 H2CO3 + 2OH- H2CO3 + 2OH- |
D.Br- + H2O 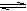 HBr + OH- HBr + OH- |
某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH变化曲线如图所示,下列判断正确的是
| A.a、c两点溶液的导电能力相同 |
| B.b点溶液中c(H+)+c(NH3·H2O)=c(OH-) |
| C.a、b、c三点溶液中水的电离程度a>b>c |
| D.用等浓度NaOH溶液和等体积b、c处溶液反应,消耗NaOH溶液体积Vb=Vc |
25℃时,取浓度均为0.1 mol/L的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol/LNaOH溶液、0.1 mol/L盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。下列说法正确的是( )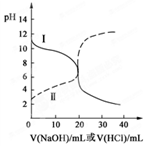
| A.曲线Ⅰ:滴加溶液到10 mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| B.曲线Ⅰ:滴加溶液到20 mL时: c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| C.曲线Ⅱ:滴加溶液在10 mL~20 mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) |
| D.曲线Ⅱ:滴加溶液到10 mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] |
某温度下,向一定体积0.1mol/L醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH( pOH=-lgc(OH-) )与pH的变化关系如图所示,则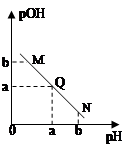
| A.N点所示溶液中c(H+) < c(OH-) |
| B.M点所示溶液导电能力强于Q点 |
| C.M点水的电离程度大于N点 |
| D.Q点消耗NaOH溶液的体积等于醋酸溶液的体积 |
在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH-离子浓度分别为A mol·L-1与B mol·L-1,则A和B的关系为
| A.A>B | B.A=10-4B | C.B=10-4A | D.A=B |
为了使FeCl3溶液中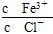 增大,可加入的物质是( )
增大,可加入的物质是( )
| A.适量的HCl气体 | B.适量的硫酸氢钠 |
| C.适量的NaOH固体 | D.适量的NaHCO3溶液 |
室温下,取0.2 mol·L-1CH3COOH溶液与0.2 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,则下列说法(或关系式)正确的是 ( )
| A.混合溶液中由水电离出的c(H+)=10-8 mol·L-1 |
| B.溶液中离子浓度由大到小的顺序为c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
| C.混合溶液中c(Na+)=c(CH3COOH)+c(CH3COO-)=0.2 mol·L-1 |
| D.混合溶液中c(OH-)-c(CH3COOH)=c(H+)=1×10-8 mol·L-1 |