题目内容
17.某药物G的合成路线如下图所示,已知一元醇A中氧的质量分数约为26.7%,E中核磁共振氢谱为四组峰,且峰面积比为2:2:2:1.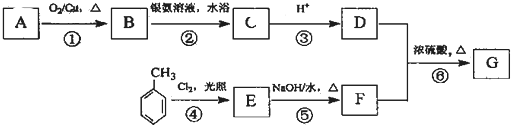
请回答下列问题:
(1)A的分子式为C3H8O;结构分析显示A只有一个甲基,A的名称为1-丙醇.
(2)上述①~⑥步中,属于氧化反应的是①②(填序号);B中所含官能团的结构简式为-CHO_.
(3)写出下列反应的化学方程式:
①E→F:
 ;
;②D+F→G:
 .
.(4)F所有同分异构体中,同时符合下列条件的有3种,任写出其中一种的结构简式:
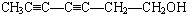 或
或 或
或 .
.a.分子中有6个碳原子在一条直线上;b.分子中含有一个羟基.
分析 一元醇A中氧的质量分数约为26.7%,设该一元醇的化学式为CnH2n+2O,氧元素的质量分数=$\frac{16}{12n+2n+2+18}$×100%=26.7%,得n=3,所以分子式为:C3H8O,A可连续被氧化,说明B为醛,D为酸,则A应为CH3CH2CH2OH,B为CH3CH2CHO,C为CH3CH2COONH4,D为CH3CH2COOH,由反应④以及E中核磁共振氢谱为四组峰,且峰面积比为2:2:2:1,可知E为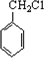 ,F为
,F为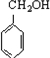 ,则G为
,则G为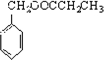 ,结合对应物质的结构和性质以及题目要求解答该题.
,结合对应物质的结构和性质以及题目要求解答该题.
解答 解:一元醇A中氧的质量分数约为26.7%,设该一元醇的化学式为CnH2n+2O,氧元素的质量分数=$\frac{16}{12n+2n+2+18}$×100%=26.7%,得n=3,所以分子式为:C3H8O,A可连续被氧化,说明B为醛,D为酸,则A应为CH3CH2CH2OH,B为CH3CH2CHO,C为CH3CH2COONH4,D为CH3CH2COOH,由反应④以及E中核磁共振氢谱为四组峰,且峰面积比为2:2:2:1,可知E为 ,F为
,F为 ,则G为
,则G为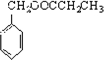 ,
,
(1)由以上分析可知A为C3H8O,结构分析显示A只有一个甲基,则A为CH3CH2CH2OH,名称为:1-丙醇;故答案为:C3H8O;1-丙醇;
(2)属于氧化还原反应的有①②,为醇、醛的氧化反应,其它为取代反应,B为CH3CH2CHO,含有的官能团为-CHO,故答案为:①②;-CHO;
(3)①E→F的反应为 的水解反应,方程式为
的水解反应,方程式为 ,
,
故答案为: ;
;
②D+F→G的反应为酯化反应,方程式为 ,
,
故答案为: ;
;
(4)F为 ,同分异构体中同时符合下列条件的有a.分子中有6个碳原子在一条直线上,则为碳碳三键结构 b.分子中含有一个羟基,则可能的结构有
,同分异构体中同时符合下列条件的有a.分子中有6个碳原子在一条直线上,则为碳碳三键结构 b.分子中含有一个羟基,则可能的结构有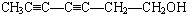 或
或 或
或 共3种;
共3种;
故答案为:3;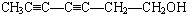 或
或 或
或 ;
;
点评 本题考查有机物的推断和合成,为高频考点,侧重学生的分析能力的考查,题目较为综合,有一定的难度,做题时注意把利用好题给信息,采用正逆推相结合的方法推断,注意同分异构体的判断方法.

 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案| A. | 取少量硫酸亚铁铵品体溶于水,先加入氯水,再滴入几滴硫氰化钾溶液,溶液变血红色,则可证明品体的成分中含有Fe2+ | |
| B. | 用到金属钠时,要用镊子取,再用小刀切下所需量,剩余钠不能放回原试剂瓶中 | |
| C. | 用pH计分别测定0.1mol•L-1的FeCl3和0.01mol•L-1FeCl3的pH,可以比较浓度对盐类水解程度的影响 | |
| D. | 通过测定等物质的量浓度的NaCl、Na2S溶液的pH,比较硫、氯两种元素的非金属性强弱 |
| A. | 1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA | |
| B. | 将1mol氯气通入足量水中发生反应转移电子数为 NA | |
| C. | 585 g氯化钠晶体中约含有6.02×1022个氯化钠分子 | |
| D. | 常温下,200 ml、0.5 mol•L-1的Na2CO3溶液中阴离子数目等于0.1 NA |
| A. | 用H2O,C2H6表示的物质一定是纯净物 | |
| B. | 氯化钡的分子式BaCl2可以表示其组成 | |
| C. | 胶体区别于其它分散系的本质特征是丁达尔现象 | |
| D. | 质子数,中子数,电子数都相同的微粒一定是同一种粒子 |

| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,碳棒上发生的反应为:Cu2++2e-═Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 | |
| D. | a和b分别连接直流电源正、负极,在电路中通过0.5mol电子后反接,又通过1mol电子,此时溶液中的c(H+)是2mol•L-1(假定溶液体积不变) |
 化合物AX3和单质X2在一定条件下反应可生成化合物AX5,该反应不能彻底.回答下列问题:
化合物AX3和单质X2在一定条件下反应可生成化合物AX5,该反应不能彻底.回答下列问题: