题目内容
配制0.1mol/LCuSO4溶液,可采用的方法是( )
| A、将25g胆矾溶于1L水中 |
| B、将25g胆矾溶于水,配成1L溶液 |
| C、取16g胆矾溶于水,再稀释到1L |
| D、称取16g无水CuSO4,溶于水配成1L溶液 |
考点:溶液的配制
专题:计算题
分析:配制1L0.10mol/L CuSO4溶液,n(CuSO4)=0.1mol,可用CuSO4或CuSO4?5H2O进行配制,质量分别为m(CuSO4)=0.1mol×160g/mol=16g,m(CuSO4?5H2O)=0.1mol×250g/mol=25g,最后加水使溶液的体积为1L.
解答:
解:A.将25g胆矾溶于1L水中,溶剂水的体积为1L,则溶液的体积大于1L,所配溶液的浓度不等于0.1mol/L,故A错误;
B.配制1L0.10mol/L CuSO4溶液,n(CuSO4)=0.1mol,m(CuSO4?5H2O)=0.1mol×250g/mol=25g,配成1L溶液,则溶液的体积为1L,可以得到0.1mol/LCuSO4溶液,故B正确;
C.配制1L0.10mol/L CuSO4溶液,n(CuSO4)=0.1mol,m(CuSO4?5H2O)=0.1mol×250g/mol=25g,故C错误;
D.配制1L0.10mol/L CuSO4溶液,n(CuSO4)=0.1mol,m(CuSO4)=0.1mol×160g/mol=16g,溶于水配成1L溶液则溶液的体积为1L,可以得到0.1mol/LCuSO4溶液,故D正确;
故选BD.
B.配制1L0.10mol/L CuSO4溶液,n(CuSO4)=0.1mol,m(CuSO4?5H2O)=0.1mol×250g/mol=25g,配成1L溶液,则溶液的体积为1L,可以得到0.1mol/LCuSO4溶液,故B正确;
C.配制1L0.10mol/L CuSO4溶液,n(CuSO4)=0.1mol,m(CuSO4?5H2O)=0.1mol×250g/mol=25g,故C错误;
D.配制1L0.10mol/L CuSO4溶液,n(CuSO4)=0.1mol,m(CuSO4)=0.1mol×160g/mol=16g,溶于水配成1L溶液则溶液的体积为1L,可以得到0.1mol/LCuSO4溶液,故D正确;
故选BD.
点评:本题考查硫酸铜溶液的配制,题目难度不大,注意溶剂的体积不等于溶液的体积,可用CuSO4或CuSO4?5H2O进行配制,注意所取溶质的质量.

练习册系列答案
相关题目
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、 制取干燥的氨气 |
B、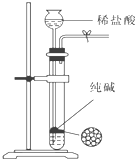 可用于制取少量纯净的CO2气体 |
C、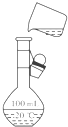 将溶液定容到100mL |
D、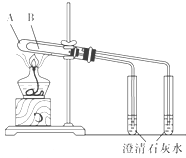 可用于比较碳酸钠和碳酸氢钠的热稳定性,大试管A中装碳酸钠固体,小试管B中装碳酸氢钠固体 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、18g D2O中含有质子的数目为NA |
| B、0.1molCl2完全反应,转移的电子数一定为0.2NA |
| C、室温下,46 g NO2和N2O4的混合气体中含有氮原子数为NA |
| D、1 L 1mol?L-1的Na2CO3溶液中,阴离子总数为NA |
下列行为中符合安全要求的是( )
| A、进入煤矿井时,用火把照明 |
| B、用点燃的火柴在液化气钢瓶口检验是否漏气 |
| C、实验桌上的酒精灯倾倒了燃烧起来,马上用湿抹布扑灭 |
| D、实验时,将水倒入浓硫酸中配制稀硫酸 |
下列说法不正确的是( )
| A、所有的复分解反应都是非氧化还原反应 |
| B、液氨、液氯、液态氯化氢都是非电解质 |
| C、静电除尘利用了胶体能发生电泳的性质 |
| D、使空气中游离态的氮转化为含氮化合物的方法叫做氮的固定 |
已知核电荷数为118的一种原子的质量数为293,则该原子中中子数与电子数之差是( )
| A、0 | B、57 | C、118 | D、175 |
下列说法中,正确的是( )
| A、1mol任何气体的体积都约是22.4 L |
| B、常温下,28 g氮气所含的原子数目为NA |
| C、在标准状况下,1mol任何物质所占的体积都约为22.4 L?mol-1 |
| D、醋酸的摩尔质量(单位为g?mol-1)与NA个醋酸分子的质量(单位为g)在数值上相等 |
下列离子方程式中正确的是( )
| A、稀硫酸与氢氧化钡溶液反应 Ba2++SO42-=BaSO4↓ |
| B、铝与氢氧溶液化钠反应 Al+2OH-=AlO2-+H2↑ |
| C、向Na2CO3浓溶液中缓慢滴加几滴稀盐酸 CO32-+H+=HCO3- |
| D、用氯化铁溶液腐蚀电路板上多余的铜 Cu+Fe3+=Cu2++Fe |