题目内容
(12分)A、B、C、D,E和F是六种短周期元素,它们的原子序数依次增大。 A和D,C与F为同主族元素;A的单质是最轻的气体; B元素最高价氧化物的水化物与其气态氢化物反应生成盐; E元素是地壳中含量最多的金属元素。F元素原子M层上电子数比L层少2个电子。 试完成下列填空
(1)E元素位于周期表的第 周期 族。
(2)F简单阴离子的结构示意图 。
(3)A、C、D 三种元素共同形成的化合物的电子式 ,其微粒间存在的化学键有 。
(4)铜与B元素最高价氧化物的水化物的稀溶液反应的离子方程式为 。
(5)E的硫酸盐溶液中滴入B元素气态氢化物的水溶液,直至过量。离子方程式为 。
【答案】
(1)3、ⅢA(2分)(2)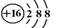 (2分)
(2分)
(3)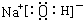 ;离子键和共价键(2分+2分)
;离子键和共价键(2分+2分)
(4)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O(2分)
(5)Al3++3NH3·H2O= 3NH4++Al(OH)3↓(2分)
【解析】最轻的单质气体是氢气,所以A是氢元素。最高价氧化物的水化物与其气态氢化物反应生成盐只有氮元素,因此B是N。地壳中含量最多的金属元素是铝,则E是Al。M层上电子数比L层少2个电子的是S,则F是S。C与F为同主族元素,所以C是O。A和D属于同一主族,且D的原子序数等于O的,所以D是Na。

练习册系列答案
相关题目
有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常见的无机试剂.E的溶质是一种无色油状液体,B、C、D和F是盐溶液,且他们的阴离子均不同.现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾
②将A为分别加入其它五种溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色,无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3沉淀均不溶.
根据上述实验信息,下列说法错误的是( )
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾
②将A为分别加入其它五种溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色,无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3沉淀均不溶.
根据上述实验信息,下列说法错误的是( )
| A、B不可能NaHCO3溶液 | B、F为AgNO3溶液 | C、D不可能是镁或铝的盐酸盐 | D、A为氨水,E为硫酸 |
