题目内容
下列有关比较正确的是( )
| A、离子半径:Na+>O2->F- |
| B、最高正价:F>O>N |
| C、第一电离能:Na<Mg<Al |
| D、电负性:S<Cl<F |
考点:元素周期律的作用,元素电离能、电负性的含义及应用
专题:元素周期律与元素周期表专题
分析:A.电子层结构相同的离子,离子半径随着原子序数增大而减小;
B.F和O一般无正价,N的最高价为+5价;
C.镁的外围电子排布式为3s2比铝的3s23p1稳定,
D.同周期从左到右电负性依次增大.
B.F和O一般无正价,N的最高价为+5价;
C.镁的外围电子排布式为3s2比铝的3s23p1稳定,
D.同周期从左到右电负性依次增大.
解答:
解:A.电子层结构相同的离子,离子半径随着原子序数增大而减小,所以离子半径:O2->F->Na+,故A错误;
B.F和O一般无正价,N的最高价为+5价,故B错误;
C.由于镁的外围电子排布式为3s2比铝的3s23p1稳定,故第一电离能:Na<Al<Mg,故C错误;
D.同周期从左到右电负性依次增大,故电负性:S<Cl<F,故D正确;
故选D.
B.F和O一般无正价,N的最高价为+5价,故B错误;
C.由于镁的外围电子排布式为3s2比铝的3s23p1稳定,故第一电离能:Na<Al<Mg,故C错误;
D.同周期从左到右电负性依次增大,故电负性:S<Cl<F,故D正确;
故选D.
点评:本题考查元素周期律的应用、电离能和电负性的比较等,难度中等.要注意镁的外围电子排布式为3s2比铝的3s23p1稳定是易错点.

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1 mol Na2O2与水完全反应时转移电子的数目为NA |
| B、标准状况下,22.4 L水中含有水分子的数目为NA |
| C、将0.1 mol FeCl3水解制成胶体,所得胶体粒子数为0. 1NA |
| D、1 L 0.1 mol?L-1乙酸溶液中H+数为0.1NA |
下列离子方程式中,属于水解反应的是( )
| A、CH3COOH+H2O?CH3COO-+H3O+ |
| B、CO2+H2O?HCO3-+H+ |
| C、CO32-+H2O?HCO3-+OH- |
| D、HS-+H2O?S2-+H3O+ |
只能表示一个化学反应的离子方程式的是( )
| A、Cu(OH)2+2HCl═CuCl2+2H2O Cu(OH)2+2H+═Cu2++2H2O |
| B、FeSO4+Ba(OH)2═Fe(OH)2↓+BaSO4↓ Fe2++SO42-+Ba2++2OH-═Fe(OH)2↓+BaSO4↓ |
| C、Ba(OH)2+H2SO4═BaSO4↓+2H2O Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
| D、2HCl+Fe(OH)2═Fe2++2H2O 2H++Fe(OH)2═Fe2++2H2O |
根据生活经验,判断下列物质按酸碱性的一定顺序依次排列正确的是( )
| A、厕所清洁剂 醋 肥皂 厨房清洁剂 |
| B、醋 厕所清洁剂 肥皂 厨房清洁剂 |
| C、厕所清洁剂 厨房清洁剂 醋 肥皂 |
| D、厨房清洁剂 醋 肥皂 厕所清洁剂 |
下列关于燃烧热的说法中正确的是( )
A、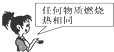 |
B、 |
C、 |
D、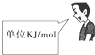 |
有M、X、Y、Z、W五种原子序数依次增大的短周期元素,其中M、Z同主族;X+与M2-具有相同的电子层结构;原子半径:Z>W;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法正确的是( )
| A、X、M两种元素形成的化合物只能存在离子键 |
| B、元素Y、Z、W的单质晶体属于同种类型的晶体 |
| C、由于W、Z、M元素的氢化物相对分子质量依次减小,所以其沸点依次降低 |
| D、元素W和M的某些单质可作为水处理中的消毒剂 |