题目内容
一定条件下存在反应:H2(g) + I2(g) 2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是
2HI(g) ΔH<0,现有三个相同的1 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol H2和1 mol I2(g),在Ⅱ中充入2 molHI(g) ,在Ⅲ中充入2 mol H2和2 mol I2(g),700 ℃条件下开始反应。达到平衡时,下列说法正确的是
A.容器Ⅰ、Ⅱ中正反应速率相同
B.容器Ⅰ、Ⅲ中反应的平衡常数相同
C.容器Ⅰ中的气体颜色比容器Ⅱ中的气体颜色深
D.容器Ⅰ中H2的转化率与容器Ⅱ中HI的转化率之和等于1
C
【解析】
试题分析:A.容器Ⅰ从正反应方向开始,开始时正反应速率最大,容器Ⅱ从逆反应方向开始,开始时正反应速率最小,是0.因此开始时正反应速率不相同,错误;B.增大压强平衡不发生移动,但是由于反应是在恒容绝热的环境中进行,当反应达到平衡时容器Ⅰ、Ⅲ中温度不等,二者的反应的平衡常数就不相同,错误;C.该反应的正反应是放热反应,随着反应的进行,反应容器的温度升高,由于升高温度,平衡向吸热的逆反应方向移动,而容器Ⅱ是从逆反应方向开始,随着反应的进行,容器内的温度逐渐降低,根据平衡移动原理:降低温度,平衡向放热的正反应方向移动,因此容器Ⅰ中的I2气体的物质的量比容器Ⅱ高,所以混合气体的颜色比容器Ⅱ中的气体颜色深,正确;D.在温度不变时反应从正反应方向开始与从逆反应方向开始,物质的转化率的和为1,由于反应恒容绝热,所以容器Ⅰ中H2的转化率比恒温时小,容器Ⅱ中HI的转化率也比恒温是小,因此二者之和小于1,错误。
考点:考查恒容绝热条件下,从正逆相反方向开始的反应的物质的转化率、平衡含量的计算的知识。

 考前必练系列答案
考前必练系列答案(10分).苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理:
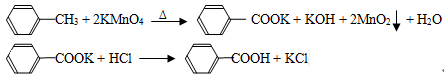
实验方法:一定量的甲苯和KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
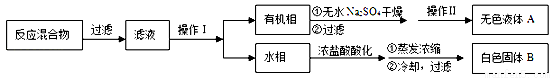
已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物都有固定熔点。
(1)操作Ⅰ为 ,操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,现象是 。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在答题卡上完成表中内容。
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体B加入水中,加热溶 解, | 得到白色晶体和无色溶液 | ----------------- |
② | 取少量滤液于试管中, | 生成白色沉淀 | 滤液含Cl— |
③ | 干燥白色晶体, | 熔点为122.4℃ | 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10—3mol,产品中苯甲酸质量分数为 (保留二位有效数字)。
 (同温同压下),此时N2、O2、CO2的物质的量之比为
(同温同压下),此时N2、O2、CO2的物质的量之比为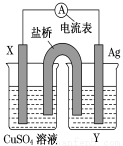
 2Fe(s) + 3CO(g) +6H2(g) ⊿H>0
2Fe(s) + 3CO(g) +6H2(g) ⊿H>0
 2NH3,该过程中还原反应的方程式为 。
2NH3,该过程中还原反应的方程式为 。
 )>c(OH
)>c(OH )> c(H+)
)> c(H+)