题目内容
2.2015年2月16日李克强总理到东北调研经济情况,重点走访了钢铁厂,鼓励钢铁厂提高钢铁质量和产量,铁及其化合物在日常生活中应用广泛.(1)利用Fe2+、Fe3+的催化作用,常温下可将SO2转化为SO42-,从而实现对SO2的治理.已知含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(2)氧化铁是重要工业颜料,下面是制备氧化铁的一种方法,其流程如下:
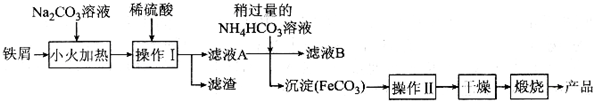
①操作Ⅰ的名称是过滤;操作Ⅱ为洗涤,洗涤操作的具体方法为沿玻璃棒往漏斗中加入适量蒸馏水至浸没沉淀,让蒸馏水自然流下,重复2-3次;
②滤液A中加入稍过量的NH4HCO3溶液生成沉淀同时有一种气体产生,写出其化学方程式:FeSO4+2NH4 HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O;
(3)如果煅烧不充分,产品中将有FeO存在,称取3.0g氧化铁产品,溶解,在250mL容量瓶中定容;量取25.00mL待测溶液于锥形瓶中,用酸化的0.01000mol/L KMnO4溶液滴定至终点,重复滴定2-3次,消耗KMnO4溶液体积的平均值为20.00mL,
①该实验中的KMnO4溶液需要酸化,用于酸化的酸是c(填字母序号).
a.稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
②计算上述产品中Fe2O3的质量分数为76%.
分析 (1)SO2转化为SO42-该过程为氧气氧化二价铁离子到三价铁离子,然后用三价铁离子氧化二氧化硫到硫酸根离子;
(2)用碳酸钠溶液除去Fe表面的油污,加稀硫酸除去碳酸钠,且溶解Fe,过除去不溶物滤,滤液A中含Fe2+,与碳酸氢铵反应生成碳酸亚铁沉淀,再过滤分离,碳酸亚铁经过洗涤、干燥、煅烧得到氧化铁;
(3)①亚铁离子具有还原性,不能用氧化性酸酸化,酸性高锰酸钾溶液具有强氧化性,不能用盐酸酸化;
②由Fe元素守恒、电子转移守恒可得关系式:5FeO~5Fe2+~KMnO4,结合关系式计算样品中FeO的质量,进而计算氧化铁的质量分数.
解答 解:(1)常温下将SO2转化为SO42-而实现SO2的处理.含SO2的废气通入含Fe2+、Fe3+的溶液时其中一个反应的离子方程式为:4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为三价铁离子氧化二氧化硫到硫酸根离子,反应的离子方程式为:2Fe3++SO2+2H20=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(2)用碳酸钠溶液除去Fe表面的油污,加稀硫酸除去碳酸钠,且溶解Fe,过除去不溶物滤,滤液A中含Fe2+,与碳酸氢铵反应生成碳酸亚铁沉淀,再过滤分离,碳酸亚铁经过洗涤、干燥、煅烧得到氧化铁.
①操作Ⅰ是分离互不相溶的固体与液态,应是过滤,操作Ⅱ为洗涤,洗涤操作的具体方法为:沿玻璃棒往漏斗中加入适量蒸馏水至浸没沉淀,让蒸馏水自然流下,重复2-3次,
故答案为:过滤;沿玻璃棒往漏斗中加入适量蒸馏水至浸没沉淀,让蒸馏水自然流下,重复2-3次;
②滤液A中含有FeSO4等,加入稍过量的NH4HCO3溶液生成碳酸亚铁沉淀,同时有一种气体产生,该气体为二氧化碳,反应化学方程式:FeSO4+2NH4 HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O,
故答案为:FeSO4+2NH4 HCO3=FeCO3↓+(NH4)2SO4+CO2↑+H2O;
(3)①亚铁离子具有还原性,硝酸具有强氧化性,不能用硝酸酸化,酸性高锰酸钾溶液具有强氧化性,不能用盐酸酸化,
故选:c;
②由Fe元素守恒、电子转移守恒可得关系式:5FeO~5Fe2+~KMnO4,
设样品中FeO的质量为m,则:
5FeO~5Fe2+~KMnO4
360g 1mol
m×$\frac{25mL}{250mL}$ 0.02L×0.01mol/L
所以 360g:m×$\frac{25mL}{250mL}$=1mol:0.02L×0.01mol/L
解得m=0.72g
则样品中氧化铁的质量分数为$\frac{3g-0.72g}{3g}$×100%=76%,
故答案为:76%.
点评 本题考查物质制备实验、定量测定实验、氧化还原反应、混合物分离提纯、实验基本操作等,需要学生熟练掌握元素化合物知识,明确工艺流程原理,为高考常考题型,是对学生综合能力的考查,题目难度中等.

| A. | 氕(${\;}_{1}^{1}$H)和氘(${\;}_{1}^{2}$H) | B. | O2和O3 | ||
| C. | 水和冰 | D. | NO和NO2 |
| A. | 置换反应 | B. | 分解反应 | C. | 化合反应 | D. | 复分解反应 |
| A. | 碱性溶液:Na+、Ca2+、SO42-、CO32- | |
| B. | 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- | |
| C. | 氯水溶液:H+、Fe2+、SO42-、Cl- | |
| D. | 含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl- |
| A | B | C |
| D |
| A. | C的非金属性最强,可与E元素形成共价化合物 | |
| B. | 元素D可形成三种价态的酸,且酸根离子均能促进水的电离 | |
| C. | 原子半径由大到小的排列顺序为:E>D>B>A>C | |
| D. | C、D元素形成的最简单的氢化物的热稳定性:D<C |
 常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH 随溶液体积变化的曲线如图所示,则下列叙述不正确的是( )
常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH 随溶液体积变化的曲线如图所示,则下列叙述不正确的是( )| A. | b、c两点溶液的导电能力不相同 | |
| B. | a、b、c三点溶液中水的电离程度a>c>b | |
| C. | 用相同浓度的盐酸分别与等体积的b、c处溶液反应,消耗盐酸体积Vb=Vc | |
| D. | c点溶液中C(H+)+C(CH3COOH)=C(OH-) |
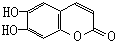 )具有抗癌作用.下列关于七叶树内酯的叙述中不正确的是( )
)具有抗癌作用.下列关于七叶树内酯的叙述中不正确的是( )| A. | 能被KMnO4酸性溶液氧化 | |
| B. | 既可以看成酚类化合物又可看成酯类化合物 | |
| C. | 能与银氨溶液发生银镜反应 | |
| D. | 1 mol该物质最多与3 mol Br2 发生反应 |
| 电化学应用 | 相关解释或说法 | |
| A | 以稀H2SO4为电解质的Cu-Zn原电池 | Cu为正极,正极上发生还原反应 |
| B | 电解CuCl2溶液 | 电子经过负极→阴极$\stackrel{通过电解液}{→}$阳极→正极 |
| C | 弱酸性环境下钢铁腐蚀 | 负极产生H2,正极处吸收O2 |
| D | 将铜闸门与外加电源负极相连 | 牺牲阳极的阴极保护法,可防止钢闸门腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
 煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题:
煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题: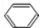 +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O;
+H2O;
 .
.