题目内容
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验).已知2KMnO4+16HCl 2KCl+2MnCl2+5Cl2↑+8H2O.
2KCl+2MnCl2+5Cl2↑+8H2O.
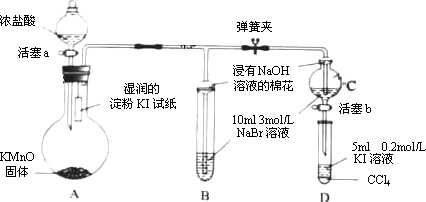
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ.打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D震荡
(1)A中产生黄绿色气体,其电子式是________.
(2)验证氯气的氧化性强于碘的实验现象是________.
(3)B、C中溶液发生反应的离子方程式是________.
(4)过程Ⅳ能证明溴的氧化性强于碘的现象是________.
(5)过程Ⅲ实验的目的是________.
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下原子半径逐渐________(填“增大”或“减少”),得电子能力逐渐减弱.
练习册系列答案
相关题目
 Br2+2Cl-(1分).
Br2+2Cl-(1分).

 为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)
为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)

