题目内容
【题目】浓度均为0.1mol/L、体积为V0的HX、HY溶液,分别加水稀释至体积V,pH随lg![]() 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是
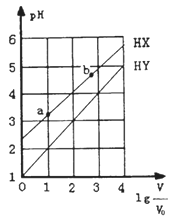
A. HX、HY都是弱酸,且HX的酸性比HY的弱
B. 相同温度下,电离常数K(HX):a>b
C. 常温下,由水电离出的c(H+)·c(OH-):a<b
D. lg![]() =3,若同时微热两种溶液,则
=3,若同时微热两种溶液,则![]() 减小
减小
【答案】C
【解析】
A.由图像可知HY溶液加水稀释104倍,溶液的PH也随之上升了4,而HX溶液的PH变化小于4,因此HY为强酸,HX为弱酸,故A项错误;B.电离平衡常数只与温度有关,因此在相同温度下,电离常数K(HX):a=b,故B项错误;C.a、b两点溶液中水的电离都是受到HX的电离的抑制的,其中在a点HX电离出的c(H+)较大,对水的电离抑制更强,因此在a点水电离出的c(H+)、c(OH-)较b点小,则有水电离出的c(H+)·c(OH-):a<b,故C项正确;D.一般情况下,升高温度,促进弱电解质的电离,因此微热两溶液时,HY是强酸,c(Y-)变化不大,而HX弱酸,c(X-)增大,则![]() 增大,故D项错误;答案选C。
增大,故D项错误;答案选C。

 小学期末标准试卷系列答案
小学期末标准试卷系列答案【题目】25℃时,有关物质的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | H2SO3 |
电离平衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)请写出H2SO3的电离平衡常数K1的表达式:________________。
(2) 常温下,将体积为10mL pH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者_____后者(填“>”、“<”或“=”)。
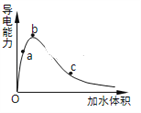
(3)一定条件下,冰醋酸加水稀释过程中溶液导电能力I随加水体积V变化曲线如右图所示,则a、b、c三点溶液醋酸的电离程度由大到小为____________________。
(4)下列离子CH3COO-、CO32-、HSO3-、SO32-在溶液中结合H+的能力由大到小的关系为___________。
(5)体积相同、c(H+)相同的①CH3COOH;②HCl;③H2SO4 三种酸溶液分别与同浓度的NaOH溶液完全中和时,消耗NaOH溶液的体积由大到小的排列顺序是_____(填序号)。
(6)已知,H+(aq) + OH-(aq) == H2O(l) ΔH =-57.3 kJ/mol。实验测得稀醋酸与稀NaOH溶液反应生成1 mol H2O时放出57 kJ的热,则醋酸溶液中,醋酸电离的热化学方程式为________________。