题目内容
同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比为________;同质量的氨气和硫化氢(H2S)气体在相同条件下的体积比为________,所含原子个数比为________;若两者所含氢原子数相等,它们的物质的量比是________.
1:2 2:1 4:3 2:3
分析:同温同压下,相同体积的任何气体含有相同数目的分子数,根据n= =
= ,结合分子的构成进行计算.
,结合分子的构成进行计算.
解答:同温同压下,气体的Vm相等,由n= =
= 可知,同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比与气体的摩尔质量成正比,则
可知,同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比与气体的摩尔质量成正比,则
m(NH3):m(H2S)=M(NH3):M(H2S)=17g/mol:34g/mol=1:2;
设气体的质量都为m,由n= =
= 可知,同质量的氨气和硫化氢(H2S)气体在相同条件下的体积比与气体的物质的量呈正比,则
可知,同质量的氨气和硫化氢(H2S)气体在相同条件下的体积比与气体的物质的量呈正比,则
v(NH3):V((H2S)=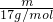 :
: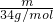 =2:1,所含原子个数比为2×4:1×3=4:3;
=2:1,所含原子个数比为2×4:1×3=4:3;
若两者所含氢原子数相等,则分子数之比为: :
: =2:3,
=2:3,
根据N=nNA可知,分子数之比等于物质的量之比,
若两者所含氢原子数相等,它们的物质的量比2:3,
故答案为:1:2;2:1;4:3;2:3.
点评:本题考查阿伏加德罗定律及推论,题目难度不大,注意物质的量的有关计算公式的运用.
分析:同温同压下,相同体积的任何气体含有相同数目的分子数,根据n=
 =
= ,结合分子的构成进行计算.
,结合分子的构成进行计算.解答:同温同压下,气体的Vm相等,由n=
 =
= 可知,同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比与气体的摩尔质量成正比,则
可知,同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比与气体的摩尔质量成正比,则m(NH3):m(H2S)=M(NH3):M(H2S)=17g/mol:34g/mol=1:2;
设气体的质量都为m,由n=
 =
= 可知,同质量的氨气和硫化氢(H2S)气体在相同条件下的体积比与气体的物质的量呈正比,则
可知,同质量的氨气和硫化氢(H2S)气体在相同条件下的体积比与气体的物质的量呈正比,则v(NH3):V((H2S)=
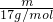 :
: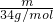 =2:1,所含原子个数比为2×4:1×3=4:3;
=2:1,所含原子个数比为2×4:1×3=4:3;若两者所含氢原子数相等,则分子数之比为:
 :
: =2:3,
=2:3,根据N=nNA可知,分子数之比等于物质的量之比,
若两者所含氢原子数相等,它们的物质的量比2:3,
故答案为:1:2;2:1;4:3;2:3.
点评:本题考查阿伏加德罗定律及推论,题目难度不大,注意物质的量的有关计算公式的运用.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目

