题目内容
(1)同温同压下,同体积的H2和CO2物质的量之比为
(2)用化学用语表示下列过程:用离子方程式表示铝粉与氢氧化钠溶液的反应
用化学方程式表示铁和水蒸气的反应,并用双线桥标出电子转移的方向和数目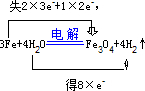

用离子方程式表示钠与水的反应,并用单线桥标出电子转移的方向和数目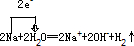
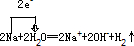 .
.
1:1
1:1
,原子个数之比为2:3
2:3
,质量比为(最简整数比)22
22
.(2)用化学用语表示下列过程:用离子方程式表示铝粉与氢氧化钠溶液的反应
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
用化学方程式表示铁和水蒸气的反应,并用双线桥标出电子转移的方向和数目


用离子方程式表示钠与水的反应,并用单线桥标出电子转移的方向和数目
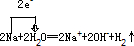
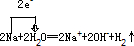
分析:(1)同温同压下,同体积的H2和CO2,其物质的量相同,然后利用构成来分析原子个数比,再利用m=n×M来计算质量比;
(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,铁和水蒸气反应生成四氧化三铁和氢气,钠与水反应生成氢氧化钠和氢气,利用化合价的变化来分析电子转移的数目,并利用单质、氧化物、气体等在离子方程式中保留化学式来分析离子方程式的书写.
(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,铁和水蒸气反应生成四氧化三铁和氢气,钠与水反应生成氢氧化钠和氢气,利用化合价的变化来分析电子转移的数目,并利用单质、氧化物、气体等在离子方程式中保留化学式来分析离子方程式的书写.
解答:解:(1)因同温同压下,同体积的H2和CO2,其物质的量相同,则其物质的量之比为1:1,
原子个数比为1×2:1×3=2:3,
其质量比为1×2:1×44=1:22,
故答案为:1:1;2:3;1:22;
(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,其离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,
铁和水蒸气反应生成四氧化三铁和氢气,反应为3Fe+4H2O
Fe3O4+4H2↑,转移的电子数为8e-,
双线桥标出电子转移的方向和数目为 ,
,
钠与水反应生成氢氧化钠和氢气,其离子反应为2Na+2H20═2Na++2OH-+H2↑,该反应中钠失去电子,氢得到电子,
则单线桥标出电子转移的方向和数目为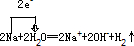 ,
,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑; ;
;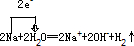 .
.
原子个数比为1×2:1×3=2:3,
其质量比为1×2:1×44=1:22,
故答案为:1:1;2:3;1:22;
(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,其离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,
铁和水蒸气反应生成四氧化三铁和氢气,反应为3Fe+4H2O
| ||
双线桥标出电子转移的方向和数目为
 ,
,钠与水反应生成氢氧化钠和氢气,其离子反应为2Na+2H20═2Na++2OH-+H2↑,该反应中钠失去电子,氢得到电子,
则单线桥标出电子转移的方向和数目为
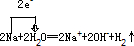 ,
,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
 ;
;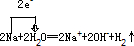 .
.点评:本题较难,考查阿伏伽德罗定律及氧化还原反应、离子反应,明确离子方程式的书写方法及标电子转移的方向和数目是解答本题的关键.

练习册系列答案
相关题目