题目内容
一定条件下,用甲烷可以消除氮氧化物(NOx)的污染.已知:
①CH4 (g)+4NO2 (g)=4NO (g)+CO2 (g)+2H2O (g);△H=-574kJ?mol-1
②CH4 (g)+4NO (g)=2N2 (g)+CO2 (g)+2H2O (g);△H=-1160kJ?mol-1.
下列选项正确的是( )
①CH4 (g)+4NO2 (g)=4NO (g)+CO2 (g)+2H2O (g);△H=-574kJ?mol-1
②CH4 (g)+4NO (g)=2N2 (g)+CO2 (g)+2H2O (g);△H=-1160kJ?mol-1.
下列选项正确的是( )
分析:A、利用盖斯定律计算CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)的反应热,根据水的状态不同,放出的热量不同判断;
B、根据CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)的反应热计算;
C、根据化合价的变化计算反应转移的电子的物质的量;
D、根据化合价的变化计算.
B、根据CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)的反应热计算;
C、根据化合价的变化计算反应转移的电子的物质的量;
D、根据化合价的变化计算.
解答:解:A、利用盖斯定律,将题中反应
可得:
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJ?mol-1,气态水变为液态水是要放热,则
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l);△H<-867kJ?mol-1,故A错误;
B、若0.2molCH4还原NO2至N2,在上述条件下放出的热量为0.2mol×867kJ?mol-1=173.4kJ,故B正确;
C、由于CH4和NOx物质的量不确定,不一定为1mol,则转移的电子的物质的量不确定,故C错误;
D、若用标准状况下2.24LCH4还原NO2至N2,整个过程中转移的电子为
×[+4-(-4)]=0.8mol,故D错误.
故选B.
| ①+② |
| 2 |
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g);△H=-867kJ?mol-1,气态水变为液态水是要放热,则
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l);△H<-867kJ?mol-1,故A错误;
B、若0.2molCH4还原NO2至N2,在上述条件下放出的热量为0.2mol×867kJ?mol-1=173.4kJ,故B正确;
C、由于CH4和NOx物质的量不确定,不一定为1mol,则转移的电子的物质的量不确定,故C错误;
D、若用标准状况下2.24LCH4还原NO2至N2,整个过程中转移的电子为
| 2.24L |
| 22.4L/moL |
故选B.
点评:本题考查化学反应热的计算以及氧化还原反应等知识,题目难度不大,注意水的状态不同,放出的热量不同,掌握利用盖斯定律计算反应热的方法.

练习册系列答案
相关题目
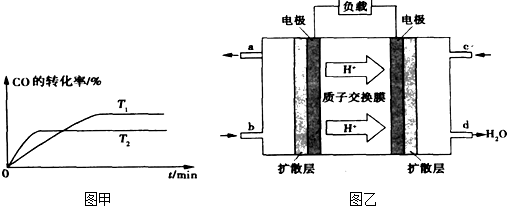
 );尿素在尿素酶的催化下跟水反应可生成碳酸铵,被作物吸收。
);尿素在尿素酶的催化下跟水反应可生成碳酸铵,被作物吸收。 );尿素在尿素酶的催化下跟水反应可生成碳酸铵,被作物吸收。
);尿素在尿素酶的催化下跟水反应可生成碳酸铵,被作物吸收。