题目内容
20.设NA为阿伏加德罗常数的数值.下列说法正确的是( )| A. | 80mL 10mol•L-1 盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA | |
| B. | 2 L0.5 mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| C. | 标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl-和ClO-两种粒子数之和为NA | |
| D. | 标准状况下,11.2LSO3所含的分子数大于0.5NA |
分析 A、二氧化锰只能与浓盐酸反应,与稀盐酸不反应;
B、求出硫酸钾的物质的量,然后根据1mol硫酸钾中含1mol硫酸根、而溶液中除了硫酸根还有水电离出的氢氧根来分析;
C、氯气和水的反应为可逆反应;
D、标况下,三氧化硫为固体.
解答 解:A、二氧化锰只能与浓盐酸反应,与稀盐酸不反应,故盐酸不能反应完,则生成的氯气分子个数小于0.2NA个,故A错误;
B、溶液中硫酸钾的物质的量n=CV=0.5mol/L×2L=1mol,而1mol硫酸钾中含1mol硫酸根,故带2mol负电荷,而溶液中除了硫酸根还有水电离出的氢氧根,故溶液中负电荷的个数大于2NA个,故B错误;
C、氯气和水的反应为可逆反应,不能进行彻底,故C错误;
D、标况下,三氧化硫为固体,故11.2L三氧化硫固体的物质的量大于0.5mol,则分子个数大于0.5NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
8.下列说法中错误的是( )
| A. | 弱电解质的电离是一个吸热过程,升温其电离度增大 | |
| B. | 某些盐类的水解是一个吸热过程,升温水解程度增大 | |
| C. | 溶液的酸碱性取决于溶液中氢离子浓度的大小 | |
| D. | 酸性溶液不一定是酸溶液,碱性溶液不一定是碱溶液 |
15.下列叙述中正确的是( )
| A. | 电能是二级能源 | B. | 水力是二级能源 | ||
| C. | 天然气是二级能源 | D. | 焦炉气是一级能源 |
12.在水中加入等物质的量的Ag+、Ba2+、Na+、SO42-、NO3-、Cl-.该溶液放在用惰性材料作电极的电解槽中,通电片刻,则氧化产物和还原产物的质量比为( )
| A. | 35.5:108 | B. | 16:137 | C. | 8:1 | D. | 108:35.5 |
9.据法国《科学与未来》杂志报道,美国科学家最近在实验室中合成了与脱氧核糖核酸(DNA)分子结构相近的苏糖核酸分子.一些专家认为这种物质包含遗传信息,可能是第三种遗传分子.苏糖核酸简称TNA,是DNA和RNA的“近亲”.TNA中含有苏糖的结构单元.已知苏糖的结构简式为:CH2OHCHOHCHOHCHO,以下有关苏糖的说法中不正确的是( )
| A. | 苏糖能发生银镜反应 | |
| B. | 苏糖与甲酸甲酯含碳的质量分数相同 | |
| C. | 苏糖在一定条件下能发生取代反应 | |
| D. | 苏糖与葡萄糖互为同分异构体 |
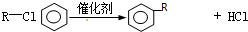
 苯甲酸是一种重要的化工产品,某学习小组设计方案制备苯甲酸.反应原理如下:
苯甲酸是一种重要的化工产品,某学习小组设计方案制备苯甲酸.反应原理如下: +2KMnO4$\stackrel{△}{→}$
+2KMnO4$\stackrel{△}{→}$ +KOH+2MnO2+H2O
+KOH+2MnO2+H2O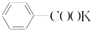 +HCl→
+HCl→ +KCl
+KCl


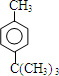 ;E
;E .
. .
. .
.