题目内容
根据如图1所示的关系,确定A、B、C、D、E、F的化学式,并写有关方程式.

(1)已知A为单质,则A为 (填化学式,下同),E为 .
(2)D→E的化学方程式为 .
(3)取少量C溶于水,加入酸化的硝酸银溶液,有白色沉淀生成,则A→C的化学方程式为 .
(4)某学习小组设计如下装置如图2进行相关实验:
①打开活塞b,向溶液B中逐滴加入少量溴水,关闭活塞b;
②打开活塞a,向容器中滴入足量的亚硫酸.
按要求回答下列问题:
①滴入溴水时,溶液的颜色变为棕黄色,该反应的离子方程式为 .
②滴入亚硫酸时,溶液由棕黄色变为浅绿色,该反应的离子方程式为 .
③由此可知,B中的阳离子、Br-、H2SO3还原性由强到弱的顺序是 (B中的阳离子用离子符号表示).

(1)已知A为单质,则A为
(2)D→E的化学方程式为
(3)取少量C溶于水,加入酸化的硝酸银溶液,有白色沉淀生成,则A→C的化学方程式为
(4)某学习小组设计如下装置如图2进行相关实验:
①打开活塞b,向溶液B中逐滴加入少量溴水,关闭活塞b;
②打开活塞a,向容器中滴入足量的亚硫酸.
按要求回答下列问题:
①滴入溴水时,溶液的颜色变为棕黄色,该反应的离子方程式为
②滴入亚硫酸时,溶液由棕黄色变为浅绿色,该反应的离子方程式为
③由此可知,B中的阳离子、Br-、H2SO3还原性由强到弱的顺序是
考点:无机物的推断,性质实验方案的设计
专题:
分析:根据题中各物质的转化关系,D与氧气反应得红褐色固体E,则E为Fe(OH)3,D为Fe(OH)2,根据D可推得B为含有Fe2+的溶液,A为单质,则A为Fe,根据E可推得C含有Fe3+,取少量C溶于水,加入酸化的硝酸银溶液,有白色沉淀生成,则C为FeCl3,在亚铁盐溶液中加入溴,可以将亚铁离子氧化成铁离子,铁离子能氧化亚硫酸,据此答题.
解答:
解:根据题中各物质的转化关系,D与氧气反应得红褐色固体E,则E为Fe(OH)3,D为Fe(OH)2,根据D可推得B为含有Fe2+的溶液,A为单质,则A为Fe,根据E可推得C含有Fe3+,取少量C溶于水,加入酸化的硝酸银溶液,有白色沉淀生成,则C为FeCl3,在亚铁盐溶液中加入溴,可以将亚铁离子氧化成铁离子,铁离子能氧化亚硫酸,
(1)根据上面的分析可知,A为Fe,E为Fe(OH)3,
故答案为:Fe;Fe(OH)3;
(2)D→E的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)A→C的化学方程式为2Fe+3Cl2
2FeCl3,
故答案为:2Fe+3Cl2
2FeCl3;
(4)①滴入溴水时,溶液的颜色变为棕黄色,该反应的离子方程式为2Fe2++Br2=2Fe3++2Br-,
故答案为:2Fe2++Br2=2Fe3++2Br-;
②滴入亚硫酸时,溶液由棕黄色变为浅绿色,该反应的离子方程式为2Fe3++H2SO3=2Fe2++SO42-+2H+,
故答案为:2Fe3++H2SO3=2Fe2++SO42-+2H+;
③根据氧化还原反应中还原剂的还原性强于还原产物可知,B中的阳离子、Br-、H2SO3还原性由强到弱的顺序是H2SO3>Fe2+>Br-,
故答案为:H2SO3>Fe2+>Br-.
(1)根据上面的分析可知,A为Fe,E为Fe(OH)3,
故答案为:Fe;Fe(OH)3;
(2)D→E的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)A→C的化学方程式为2Fe+3Cl2
| ||
故答案为:2Fe+3Cl2
| ||
(4)①滴入溴水时,溶液的颜色变为棕黄色,该反应的离子方程式为2Fe2++Br2=2Fe3++2Br-,
故答案为:2Fe2++Br2=2Fe3++2Br-;
②滴入亚硫酸时,溶液由棕黄色变为浅绿色,该反应的离子方程式为2Fe3++H2SO3=2Fe2++SO42-+2H+,
故答案为:2Fe3++H2SO3=2Fe2++SO42-+2H+;
③根据氧化还原反应中还原剂的还原性强于还原产物可知,B中的阳离子、Br-、H2SO3还原性由强到弱的顺序是H2SO3>Fe2+>Br-,
故答案为:H2SO3>Fe2+>Br-.
点评:本题考查无机物的推断,注意物质的颜色为解答本题的突破口,熟悉铁及其化合物的性质即可解答,注意氧化还原反应,题目难度不大.

练习册系列答案
相关题目
某课外活动小组的同学从某地颗粒采集器中获得雾霾颗粒样品,然后用蒸馏水浸取.在探究雾霾颗粒可溶性成分的实验中,下列根据实验现象得出的结论不正确的是( )
| A、向浸取液中滴入AgNO3溶液有白色沉淀产生,说明雾霾中一定含有Cl- |
| B、向浸取液中滴入硝酸酸化的BaCl2溶液,有白色沉淀产生,说明雾霾中一定含SO42- |
| C、向浸取液中加入Cu和浓H2SO4,试管口有红棕色气体产生,说明雾霾中可能含有NO3- |
| D、向浸取液中加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明雾霾中一定含有NH4+ |
下列实验操作中,正确的是( )
A、 排水法收集NO |
B、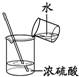 稀释浓硫酸 |
C、 实验室制氨气 |
D、 定容 |
从植物中分离出的活性化合物zeylastral的结构简式如图所示. 下列说法不正确的是( )
下列说法不正确的是( )
 下列说法不正确的是( )
下列说法不正确的是( )| A、分子中含有6个手性碳原子 |
| B、能与FeCl3溶液、银氨溶液发生反应 |
| C、1mol zeylastral最多与5molH2发生反应 |
| D、1mol zeylastral最多可与lmolBr2发生反应 |
下列气体不会造成大气污染的是( )
| A、二氧化硫 | B、一氧化氮 |
| C、一氧化碳 | D、氮气 |
下列物质在给定条件下可以直接转化的是( )
A、Al2O3
| |||||
B、Fe
| |||||
C、SiO2
| |||||
D、CaCl2
|
已知某反应的焓变小于零,则下列叙述正确的是( )
| A、该反应一定是放热反应 |
| B、该反应一定是吸热反应 |
| C、该反应中反应物的总能量一定小于产物的总能量 |
| D、该反应中反应物的总能量一定大于产物的总能量 |
NA表示阿伏加德罗常数.下列叙述正确的是( )
| A、1.2g金刚石中含有的碳碳单键数为0.4NA |
| B、300 mL 2 mol/L乙醇水溶液中所含H原子数为3.6NA |
| C、2.3 g钠在O2中充分反应得到3.5 g固体,转移电子数为0.15NA |
| D、标准状况下,22.4 L丙烯中含有碳氢键数为6NA |