��Ŀ����
3��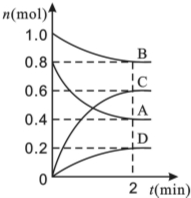 T��ʱ�����ݻ�Ϊ0.5L���ܱ������з���ijһ��Ӧ���Ҳ�ò�ͬʱ����������������A��B��C��D�����ʵ����仯��ͼ��ʾ����֪������A��B��C��Ϊ��̬��DΪ��̬������Ӧʱ���ȷ�Ӧ������Ҫ��ش��������⣺
T��ʱ�����ݻ�Ϊ0.5L���ܱ������з���ijһ��Ӧ���Ҳ�ò�ͬʱ����������������A��B��C��D�����ʵ����仯��ͼ��ʾ����֪������A��B��C��Ϊ��̬��DΪ��̬������Ӧʱ���ȷ�Ӧ������Ҫ��ش��������⣺��1�������з�Ӧ�Ļ�ѧ����ʽΪ
2A+B?3C+D
��2��ǰ2 min��v��A��=0.4mol•��min•L��-1��
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����D��
A����������ѹǿ����
B�����������ܶȲ���
C������0.1mol��Bͬʱ����0.1mol��D
D��B�����ʵ�������
��4��T��ʱ���÷�Ӧ��ƽ�ⳣ��K=1.69������С�������λ����
��5����Ӧ�ﵽƽ��ı����д�ʩ��ʹA��ת�����������C����ѡ����ĸ����
A��ֻ����A�����ʵ��� B������һ����D
C�����߷�Ӧ��ϵ���¶� D���������������Сһ��
��6��T��ʱ���ݻ�Ϊ1 L���ܱ������У���ʼʱ����0.2 mol A��0.4 mol B��0.3 mol C��0.5 mol D����ʱv��������v���棩���������������=������
���� ��1��A��B�����ʵ������٣�Ϊ��Ӧ�C��D�����ʵ������ӣ�Ϊ������ﵽƽ��ʱA��B��C��D�ı�����ʵ����ֱ�Ϊ0.4mol��0.2mol��0.6mol��0.2mol����A��B��C��D�Ļ�ѧ������֮��0.4��0.2��0.6��0.2=2��1��3��1���ʷ�Ӧ�Ļ�ѧ����ʽΪ��2A+B?3C+D��
��2������v=$\frac{��c}{��t}$����v��A����
��3�����淴Ӧ����ƽ��ʱ��ͬ�����ʵ�������������ұ��ֲ��䣬����ֵ�Ũ�ȡ��������ֲ��䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣻
��4����Ӧǰ����������ʵ������䣬�����ʵ�������Ũ�ȴ���K=$\frac{{c}^{3}��C��}{{c}^{2}��A����c��B��}$����ƽ�ⳣ����
��5������ӦΪ���������������ȷ�Ӧ���ı�����ʹA��ת��������Ӧʹƽ�������ƶ���������ֻ����A��Ũ�ȣ�DΪ���壬D�����ʵ����仯��Ӱ��ƽ���ƶ��������������¶ȡ�����C��������B��Ũ�ȣ�
��6�������ʱŨ����Qc����Qc=K������ƽ��״̬����Qc��K����Ӧ������Ӧ���У���Qc��K����Ӧ���淴Ӧ���У�
��� �⣺��1��A��B�����ʵ������٣�Ϊ��Ӧ�C��D�����ʵ������ӣ�Ϊ������ﵽƽ��ʱ����n��A��=0.8mol-0.4mol=0.4mol����n��B��=1mol-0.0mol=0.2mol����n��C��=0.6mol����n��D��=0.2mol����A��B��C��D�Ļ�ѧ������֮��Ϊ0.4��0.2��0.6��0.2=2��1��3��1���ʷ�Ӧ�Ļ�ѧ����ʽΪ��2A+B?3C+D��
�ʴ�Ϊ��2A+B?3C+D��
��2��ǰ2 min��n��A��=0.8mol-0.4mol=0.4mol����v��A��=$\frac{\frac{0.4mol}{0.5L}}{2min}$=0.4mol•��min•L��-1��
�ʴ�Ϊ��0.2��
��3��A����Ӧǰ�����������ʵ������䣬���º����£���������ѹǿʼ�ղ��䣬��A����
B������������������䣬�����ݻ����䣬���������ܶ�Ϊ��ֵ����B����
C������0.1mol��Bͬʱ����0.1mol��D������ʾ����Ӧ���ʣ���Ӧʼ�հ��ñ�����ϵ���У���C����
D�����淴Ӧ�õ�ƽ��ʱ������ֵ����ʵ������䣬B�����ʵ�������˵����Ӧ����ƽ�⣬��D��ȷ��
��ѡ��D��
��4��ƽ��ʱAΪ0.4mol��BΪ0.8mol��CΪ0.6mol����Ӧǰ����������ʵ������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ������K=$\frac{{c}^{3}��C��}{{c}^{2}��A����c��B��}$=$\frac{0��{6}^{3}}{0��{4}^{2}��0.8}$=1.69��
�ʴ�Ϊ��1.69��
��5��A��ֻ����A�����ʵ�����ƽ����Ȼ�����ƶ�����A��ת���ʼ�С����A����
B��DΪ���壬����һ����D����Ӱ��ƽ���ƶ�����B����
C������ӦΪ���ȷ�Ӧ�����߷�Ӧ��ϵ���¶ȣ�ƽ�������ƶ���A��ת��������C��ȷ��
D���������������Сһ����ѹǿ����Ӧǰ������������䣬ƽ�ⲻ�ƶ�����D����
��ѡ��C��
��6����ʱŨ����Qc=$\frac{0��{5}^{3}}{0��{2}^{2}��0.4}$=7.8��K=1.69���ʷ�Ӧ���淴Ӧ���У���v��������v���棩��
�ʴ�Ϊ������
���� ���⿼�黯ѧƽ�������Ӱ�����ء���ѧƽ��״̬�жϡ�ƽ�ⳣ�����㼰Ӧ�õȣ�ע��Ի�ѧƽ�ⳣ����������Ӧ�ã�

 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�| A�� | 0.045mol/L | B�� | 0.036mol/L | C�� | 0.026mol/L | D�� | 0.030mol/L |
��Na2O2 ��NaHCO3 ��Al��OH��3��FeCl2 ��Fe��OH��3��
| A�� | ֻ�Т٢ڢ� | B�� | ֻ�Т٢ڢܢ� | C�� | ֻ�Т٢ڢ� | D�� | ȫ�� |
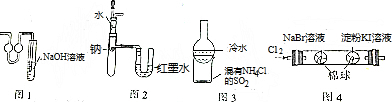
| A�� | ͼ1װ�����ڶ�������β�������� | |
| B�� | ͼ2װ��������֤Na��ˮ��Ӧ����ЧӦ | |
| C�� | ����ͼ3װ���е��ձ�������SiO2��NH4Cl | |
| D�� | ͼ4װ������֤�������ԣ�Cl2��Br2��I2 |
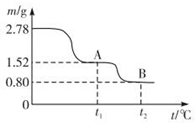 ���й��Ŵ������������̷���FeSO4•7H2OΪԭ�ϣ���������¯�ж��տ��Ƶ��̷��ͣ��̷�����һ����ɫճ��Һ�壬�����ڳ��������ϵ����⣮��ͼ��2.78g�̷������������ȷֽ�ʱ�����ù��������������¶ȱ仯�����ߣ������Ȳ�������������ͨ��������BaCl2��Һ������ɫ����1.16g��
���й��Ŵ������������̷���FeSO4•7H2OΪԭ�ϣ���������¯�ж��տ��Ƶ��̷��ͣ��̷�����һ����ɫճ��Һ�壬�����ڳ��������ϵ����⣮��ͼ��2.78g�̷������������ȷֽ�ʱ�����ù��������������¶ȱ仯�����ߣ������Ȳ�������������ͨ��������BaCl2��Һ������ɫ����1.16g��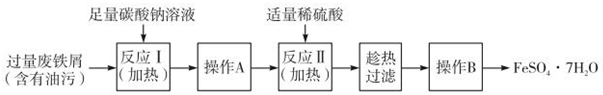
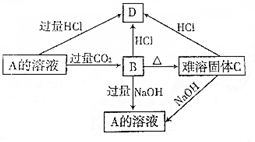
 �������䡱)��
�������䡱)��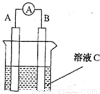
 ��ֻҪ�ѵƷ��뺣ˮ�����ӣ��ͻᷢ��ҫ�۵İ⡣���Դ�ĸ���������________��������ӦΪ___________��������ӦΪ_______________________��
��ֻҪ�ѵƷ��뺣ˮ�����ӣ��ͻᷢ��ҫ�۵İ⡣���Դ�ĸ���������________��������ӦΪ___________��������ӦΪ_______________________�� 2C(g)������2s����C��Ũ��Ϊ0.6mol��L��1���������м���˵����������ȷ����
2C(g)������2s����C��Ũ��Ϊ0.6mol��L��1���������м���˵����������ȷ����