题目内容
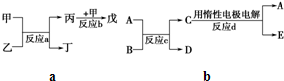
结合图2中所示转化关系回答有关问题.

(1)液态F能否导电
(2)A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占每年产量的10%.A发生腐蚀的主要原因是(填写下面的选项序号)
a.直接与氧气发生化学腐蚀
b.通过原电池反应发生腐蚀
c.因溶于水而消耗掉
①若你选定选项a或c,请写出相应的化学方程式:
②若你选定选项b,请写出负极的电极反应式
(3)气体y的密度约是空气密度的1.1倍,则沉淀x的化学式是

(4)写出D+某金属单质→B的化学方程式:

(1)液态F能否导电
否
否
(填“能”或“否”).(2)A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占每年产量的10%.A发生腐蚀的主要原因是(填写下面的选项序号)
b
b
.a.直接与氧气发生化学腐蚀
b.通过原电池反应发生腐蚀
c.因溶于水而消耗掉
①若你选定选项a或c,请写出相应的化学方程式:
不填写
不填写
;②若你选定选项b,请写出负极的电极反应式
Fe-2e-═Fe2+
Fe-2e-═Fe2+
.(①、②只答其一)(3)气体y的密度约是空气密度的1.1倍,则沉淀x的化学式是
Fe(OH)3
Fe(OH)3
.物质H的电子式

(4)写出D+某金属单质→B的化学方程式:
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
2Al+2NaOH+2H2O═2NaAlO2+3H2↑
.分析:A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占每年产量的10%,则A是铁,电解饱和食盐水生成氢氧化钠、氢气和氯气,氯气能和铁反应生成氯化铁,则C是氯气,E是氯化铁,B和C反应生成F,F能和铁反应,则B是氢气,F是氯化氢,D是氢氧化钠,氢氧化钠和金属单质铝反应生成氢气,盐酸和铁反应生成氯化亚铁和氢气,则G是氯化亚铁,氯化铁和H反应生成沉淀和气体,气体y的密度约是空气密度的1.1倍则y是氧气,H具有强氧化性,为过氧化钠.
解答:解:A是一种非常重要的工业产品.据统计,地球上每年由于腐蚀而消耗的A约占每年产量的10%,则A是铁,电解饱和食盐水生成氢氧化钠、氢气和氯气,氯气能和铁反应生成氯化铁,则C是氯气,E是氯化铁,B和C反应生成F,F能和铁反应,则B是氢气,F是氯化氢,D是氢氧化钠,氢氧化钠和金属单质铝反应生成氢气,盐酸和铁反应生成氯化亚铁和氢气,则G是氯化亚铁,氯化铁和H反应生成沉淀和气体,气体y的密度约是空气密度的1.1倍则y是氧气,H具有强氧化性,为过氧化钠.
(1)液态F是氯化氢,氯化氢中只含分子不含自由离子,所以液态氯化氢不导电,故答案为:否;
(2)生铁中含有铁和碳,铁、碳和电解质溶液能构成原电池,铁作负极而加速被腐蚀,故选b;
负极上铁失电子发生氧化反应,电极反应式为:Fe-2e-═Fe2+,
故答案为:b;Fe-2e-═Fe2+;
(3)气体y的密度约是空气密度的1.1倍,则y的相对分子质量为32,则y是氧气,H是过氧化钠,过氧化钠和水反应生成氢氧化钠,氢氧化钠和铁离子反应生成氢氧化铁,所以沉淀x的化学式是Fe(OH)3,物质H的电子式 ,
,
故答案为:Fe(OH)3;
(4)氢氧化钠溶液和铝反应生成偏铝酸钠和氢气,反应方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
(1)液态F是氯化氢,氯化氢中只含分子不含自由离子,所以液态氯化氢不导电,故答案为:否;
(2)生铁中含有铁和碳,铁、碳和电解质溶液能构成原电池,铁作负极而加速被腐蚀,故选b;
负极上铁失电子发生氧化反应,电极反应式为:Fe-2e-═Fe2+,
故答案为:b;Fe-2e-═Fe2+;
(3)气体y的密度约是空气密度的1.1倍,则y的相对分子质量为32,则y是氧气,H是过氧化钠,过氧化钠和水反应生成氢氧化钠,氢氧化钠和铁离子反应生成氢氧化铁,所以沉淀x的化学式是Fe(OH)3,物质H的电子式
 ,
,故答案为:Fe(OH)3;
(4)氢氧化钠溶液和铝反应生成偏铝酸钠和氢气,反应方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
点评:本题考查无机物的推断,明确推断中转化的关系及物质的性质即可解答,明确推断突破口为A及饱和食盐水电解产物,难度中等.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目