题目内容
在下列提供的试剂中,选择合适的试剂除去下表中各混合物的杂质(括号内物质为杂质),并按要求填写空格.
A.NaOH溶液 B.氨水 C.铁粉 D.稀盐酸 E.氯水 F.溴水
A.NaOH溶液 B.氨水 C.铁粉 D.稀盐酸 E.氯水 F.溴水
| 混合物(括号内为杂质) | 除杂试剂(填序号) | 反应离子方程式 |
| ①FeCl3(FeCl2) | ||
| ②Mg(Al) | ||
| ③NaBr(NaI) | ||
| ④SiO2 (CaCO3) |
考点:物质的分离、提纯的基本方法选择与应用,离子方程式的书写,物质的分离、提纯和除杂
专题:离子反应专题
分析:①利用氯水将亚铁离子氧化可实现除杂;
②利用NaOH与Al反应,则选NaOH溶液反应后过滤可除杂;
③利用溴水与NaI反应除杂;
④碳酸钙与盐酸反应,而二氧化硅不能.
②利用NaOH与Al反应,则选NaOH溶液反应后过滤可除杂;
③利用溴水与NaI反应除杂;
④碳酸钙与盐酸反应,而二氧化硅不能.
解答:
解:①除去FeCl3中的FeCl2,选择试剂为E(氯水),发生离子反应为2Fe2++Cl2=2Fe3++2Cl-;
②除去Mg中的Al,选择试剂为A(NaOH溶液),Al反应,而Mg不能,发生的离子反应为2Al+2OH-+6H2O=2[Al(OAH)4]-+3H2↑,过滤即可除杂;
③除去NaBr中的NaI,选择试剂为F(溴水),发生的离子反应为2I-+Br2=I2+2Br-,然后萃取、分液即可除杂;
④碳酸钙与盐酸反应,而二氧化硅不能,则除去SiO2中的CaCO3,选择试剂为D(稀盐酸),发生的离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:
②除去Mg中的Al,选择试剂为A(NaOH溶液),Al反应,而Mg不能,发生的离子反应为2Al+2OH-+6H2O=2[Al(OAH)4]-+3H2↑,过滤即可除杂;
③除去NaBr中的NaI,选择试剂为F(溴水),发生的离子反应为2I-+Br2=I2+2Br-,然后萃取、分液即可除杂;
④碳酸钙与盐酸反应,而二氧化硅不能,则除去SiO2中的CaCO3,选择试剂为D(稀盐酸),发生的离子反应为CaCO3+2H+=Ca2++CO2↑+H2O,
故答案为:
| 混合物(括号内为杂质) | 除杂试剂(填序号) | 反应离子方程式 |
| ①FeCl3(FeCl2) | E | 2Fe2++Cl2=2Fe3++2Cl- |
| ②Mg(Al) | A | 2Al+2OH-+6H2O=2[Al(OAH)4]-+3H2↑ |
| ③NaBr(NaI) | F | 2I-+Br2=I2+2Br- |
| ④SiO2 (CaCO3) | D | CaCO3+2H+=Ca2++CO2↑+H2O |
点评:本题考查混合物分离提纯及方法的选择,为高频考点,把握物质的性质及差异、混合物分离提纯方法为解答的关键,侧重物质性质的考查,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、2013年冬,我国东部地区再次遭遇大范围持续雾霾天气,雾霾中的主要污染物就是二氧化硫和二氧化氮 |
| B、“臭氧空洞”“光化学烟雾”“酸雨”“温室效应”等现象都与氮氧化物有关 |
| C、“雷雨发庄稼”是因为下雷雨时空气中的氮气会被氧化,随雨水落入土壤形成氮肥 |
| D、大气中的氮氧化物主要来自于汽车尾气的排放,而汽车尾气中之所以含有氮氧化物是因为汽油燃烧不充分 |
下列离子方程式书写正确的是( )
| A、澄清的石灰水与醋酸反应:OH-+CH3COOH=CH3COO-+H2O |
| B、碳酸钙与盐酸反应:CO2-3+2H+═CO2↑+H2O |
| C、钠与水反应:Na++H2O═Na++OH-+H2↑ |
| D、铜片与硝酸银溶液反应:Cu+Ag+═Cu2++Ag |
 :
: :
: :
: :
: 是由一种单体缩聚而成的,该单体的键线式为
是由一种单体缩聚而成的,该单体的键线式为 )滴入Na2CO3溶液中发生的化学方程式:
)滴入Na2CO3溶液中发生的化学方程式: 在较高温度下和Br2按物质的量之比1:1发生加成反应的化学方程式
在较高温度下和Br2按物质的量之比1:1发生加成反应的化学方程式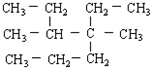 的正确系统命名为
的正确系统命名为