题目内容
 向甲、乙、丙三个恒容容器中充人一定量X和Y,发生反应X(g)+yY(g)?2Z(g).各容器中温度、反应物的起始量如下表,反应过程中Z的浓度随时问变化如图.下列说法正确的是( )
向甲、乙、丙三个恒容容器中充人一定量X和Y,发生反应X(g)+yY(g)?2Z(g).各容器中温度、反应物的起始量如下表,反应过程中Z的浓度随时问变化如图.下列说法正确的是( )| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/ | T1 | T2 | T3 |
| 反应物起始量 | 1.5mol X 0.5mol Y |
1.5mol X 0.5mol Y |
6.0mol X 2.0mol Y |
| A、20 min内,甲容器反应速率v(X)=0.075mol?L-1?min-1 |
| B、该反应温度升高.平衡常数增大 |
| C、其它条件不变,若缩小乙的体积.Y的转化率不变 |
| D、10 min时,向丙容器中再加入2mol Z,达新平衡前,v(正)、v(逆)均逐渐增大 |
分析:A、由图可知,20min内甲容器中Z的浓度变化量为1.5mol/L,根据v=
计算v(Z),再利用速率之比等于化学计量数之比计算v(X);
B、比较甲与乙可知,乙先到达平衡,故温度T1<T2,温度越高Z的浓度越低,升高温度平衡向逆反应移动;
C、根据表中乙、丙的数据,丙的体积是乙的2倍,物质的量是乙的4倍,也就是起始浓度是乙的2倍,但发现平衡时丙的浓度仍然是乙的2倍,也就是该反应是一个气体体积不变的反应;
D、化学平衡状态时,加入Z,增大了生成物浓度,而反应物浓度不变,根据浓度变化判断正逆反应速率变化.
| △c |
| △t |
B、比较甲与乙可知,乙先到达平衡,故温度T1<T2,温度越高Z的浓度越低,升高温度平衡向逆反应移动;
C、根据表中乙、丙的数据,丙的体积是乙的2倍,物质的量是乙的4倍,也就是起始浓度是乙的2倍,但发现平衡时丙的浓度仍然是乙的2倍,也就是该反应是一个气体体积不变的反应;
D、化学平衡状态时,加入Z,增大了生成物浓度,而反应物浓度不变,根据浓度变化判断正逆反应速率变化.
解答:解:A、由图可知,20min内甲容器中Z的浓度变化量为1.5mol/L,v(Z)=
=0.075mol?L-1?min-1,速率之比等于化学计量数之比,所以v(X)=
?v(Z)=0.0375mol?L-1?min-1,故A错误;
B、比较甲与乙可知,乙先到达平衡,故温度T1<T2,温度越高Z的浓度越低,升高温度平衡向逆反应移动,化学平衡常数减小,故B错误;
C、根据表中乙、丙的数据:丙的体积是乙的2倍,物质的量是乙的4倍,也就是起始浓度是乙的2倍,但发现平衡时丙的浓度仍然是乙的2倍,也就是该反应是一个气体体积不变的反应,所以若缩小乙的体积,化学平衡不移动,即Y的转化率不变,故C正确;
D、化学平衡状态时,加入Z,增大了生成物浓度,而反应物浓度不变,瞬间v(逆)增大,v(正)不变,而建立新平衡过程中,v(逆)逐渐减小,v(正)逐渐增大,故D错误;
故选C.
| 1.5mol/L |
| 20min |
| 1 |
| 2 |
B、比较甲与乙可知,乙先到达平衡,故温度T1<T2,温度越高Z的浓度越低,升高温度平衡向逆反应移动,化学平衡常数减小,故B错误;
C、根据表中乙、丙的数据:丙的体积是乙的2倍,物质的量是乙的4倍,也就是起始浓度是乙的2倍,但发现平衡时丙的浓度仍然是乙的2倍,也就是该反应是一个气体体积不变的反应,所以若缩小乙的体积,化学平衡不移动,即Y的转化率不变,故C正确;
D、化学平衡状态时,加入Z,增大了生成物浓度,而反应物浓度不变,瞬间v(逆)增大,v(正)不变,而建立新平衡过程中,v(逆)逐渐减小,v(正)逐渐增大,故D错误;
故选C.
点评:本题考查化学平衡移动、计算及化学平衡图象,难度不大,注意理解图象的纵坐标和横坐标的意义.

练习册系列答案
相关题目
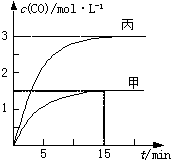 一定条件下存在反应:C(s)+H2O(g)═CO(g)+H2(g)△H>0.向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图.
一定条件下存在反应:C(s)+H2O(g)═CO(g)+H2(g)△H>0.向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图.| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | V |
| 温度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2molC 1molH2O |
1molCO 1molH2 |
4molC 2molH2O |
| A、甲容器中,反应在前15 min的平均速率v(H2)=0.1 mol?L-1?min-1 |
| B、丙容器的体积V<0.5 L |
| C、当温度为T1℃时,反应的平衡常数K=2.25 |
| D、乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2 |
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)汽车尾气中CO、NO2气体在一定条件下可以发生反应:
4CO(g)+2NO2(g)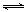 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
①恒温恒容条件下,不能说明该反应已达到平衡状态的是________(填序号);
A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体密度保持不变
②能使该反应的反应速率增大,且平衡向逆反应方向移动的是________(填序号);
A.及时分离出CO2 B.适当升高温度
C.减小容器体积使体系压强增大 D.选择高效催化剂
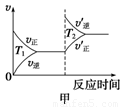
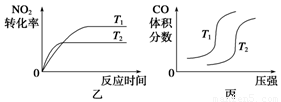
③对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是________(填序号);
(2)汽车尾气中CO与H2O(g)在一定条件下可以发生反应:CO(g)+H2O(g)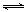 CO2(g)+H2(g) ΔH<0;820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照右表进行投料,达到平衡状态时K=1.0。
CO2(g)+H2(g) ΔH<0;820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照右表进行投料,达到平衡状态时K=1.0。
|
起始物质的量 |
甲 |
乙 |
丙 |
|
n(H2O)/mol |
0.10 |
0.20 |
0.20 |
|
n(CO)/mol |
0.10 |
0.10 |
0.20 |
①该反应的平衡常数表达式为___________;平衡时,甲容器中CO的转化率= ;
②平衡时,比较下列容器中CO的转化率:乙 甲(填“>”、“=”或“<”,下同);丙 甲。

则△H1_____0(选填“>”、“=”或“<”)。
(3)如果上述反应Ⅰ以CO和H2O(g)为起始反应物,在T℃时CO和H2O浓度变化如图所示,且密闭容器的容积为1L。那么0~4 min的平均反应速率v(CO2)=____mol/(L·min),对照“表一”可知T=______ ℃。
(3)如果上述反应Ⅰ以CO和H2O(g)为起始反应物,在T℃时CO和H2O浓度变化如图所示,且密闭容器的容积为1L。那么0~4 min的平均反应速率v(CO2)=____mol/(L·min),对照“表一”可知T=______ ℃。

(4)某温度下,反应I的化学平衡常数为2.25。在该温度下,向甲、乙、丙三个恒容密闭容器中通入CO2(g) 和H2(g),这两种物质的起始浓度如下表二:

反应速率最快的是______(填“甲”、“乙”或“丙”),平衡时,H2转化率最大的是_________(填 “甲”、“乙”或“丙”),丙中H2的转化率为__________。

 CO(g)+H2O(g) △H1
CO(g)+H2O(g) △H1  CO2(g)+H2(g) △H2
CO2(g)+H2(g) △H2