题目内容
18.火药是中国古代“四大发明”之一.黑火药爆炸时发生如下反应:2KNO3+C+S═K2S+2NO2↑+CO2↑.其中被还原的元素是N、S,被氧化的元素是C,氧化剂是KNO3、S,还原剂是C.分析 反应2KNO3+C+S═K2S+2NO2↑+CO2↑中,N和S元素化合价降低,被还原,则KNO3和硫为氧化剂,C元素化合价升高,被氧化,C为还原剂,以此解答该题.
解答 解:反应2KNO3+C+S═K2S+2NO2↑+CO2↑中,N和S元素化合价降低,被还原,则KNO3和硫为氧化剂,还原产物为K2S和N2,C元素化合价升高,被氧化,C为还原剂,CO2为氧化产物,
故答案为:N、S; C;KNO3、S; C.
点评 本题考查氧化还原反应知识,侧重于基本概念的理解,注意从元素化合价的角度分析相关概念并判断物质具有的性质,难度不大.

练习册系列答案
相关题目
3.如图所示,下列实验现象预测或操作正确的是( )
| A. | 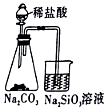 如图,可以证明非金属性强弱:Cl>C>Si | |
| B. | 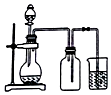 如图,用铜片和稀硝酸制NO | |
| C. | 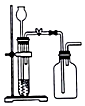 如图,用锌粒和稀硫酸制H2 | |
| D. | 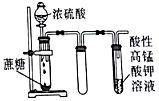 如图,酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去 |
9.用下列实验装置进行相应实验,能达到实验目的是( )


| A. | 用装置甲制取氨气 | B. | 用装置乙制取少量纯净的CO2气体 | ||
| C. | 用装置丙验证氨气具有还原性 | D. | 用装置丁吸收尾气氨气 |
6.氯化铁溶液与氢氧化铁胶体具有的共同性质是( )
| A. | 分散质颗粒直径都在l~100nm之间 | B. | 都透过半透膜 | ||
| C. | 都是透明的澄清液体 | D. | 都呈红褐色 |
13.元素的原子结构决定其性质和元素周期表中的位置,下列说法正确的是( )
| A. | 元素原子的最外层电子数等于元素的最高化合价 | |
| B. | 多电子原子中,在离核较近的区域内运动的电子能量较高 | |
| C. | S、Cl的电负性和单质的氧化性均依次增强 | |
| D. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
10.下列有关实验原理、方法和结论都正确的是( )
| A. | 除去氨气中少量水蒸汽,可以通过装有浓硫酸的洗气瓶 | |
| B. | 可用酸性KMnO4溶液鉴别CO2和SO2 | |
| C. | 加入氯水,再加入KSCN溶液,溶液显红色,则溶液中一定含有Fe2+ | |
| D. | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口如果试纸不变蓝说明原溶液中无NH4+ |
7.下列说法正确的是( )
| A. | 石英玻璃主要成分是硅酸盐 | |
| B. | 太阳能电池可采用二氧化硅材料制作,其应用有利于环保、节能 | |
| C. | 木材浸泡在硅酸钙溶液可以防腐和防火 | |
| D. | 工艺师利用氢氟酸刻蚀石英制作艺术品 |
8.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,11.2L SO3中含有的分子数为0.5NA | |
| B. | 常温下,46gNO2和N2O4的混合气体中含有原子总数为3NA | |
| C. | 1mol C10H22含共价键数目32NA | |
| D. | 1L 2mol/L的MgCl2溶液中含Mg2+数为2NA |
 ;
;