题目内容
1.某溶液中存在Na+、Ba2+、SO32-、S2-、HCO3-、Cl-、AlO2-、Br-、中的若干种,依次进行下列实验,观察到现象记录如下.(1)用pH试纸检验,溶液的pH≈7;(2)向溶液中滴加新制氯水,无气体产生,加入四氯化碳振荡、静置,四氯化碳层呈红棕色,用分液漏斗分液;(3)向分液后所得的水溶液中加入硝酸钡和稀硝酸的混合液.只有白色沉淀产生,过滤;(4)在滤液中加入硝酸银和稀硝酸的混合液,有白色沉淀产生.下列判断正确的是( )①肯定有Na+②肯定有SO42- ③肯定有SO32- ④肯定有Br- ⑤肯定有Cl- ⑥肯定没有HCO3-.
| A. | ②③④⑥ | B. | ①②④⑥ | C. | ①③④⑥ | D. | ③④⑤⑥ |
分析 (1)用pH试纸检验,溶液的pH≈7,则不含能水解显酸性或碱性的离子,如不存在S2-、HCO3-、AlO2-;
(2)向溶液中滴加新制氯水,无气体产生,加入四氯化碳振荡、静置,四氯化碳层呈红棕色,用分液漏斗分液,可知一定含Br-;
(3)向分液后所得的水溶液中加入硝酸钡和稀硝酸的混合液.只有白色沉淀产生,过滤,白色沉淀为BaSO4,则含SO32-;
(4)在滤液中加入硝酸银和稀硝酸的混合液,有白色沉淀产生白色沉淀为AgCl,但(2)中加氯水引入氯离子,以此来解答.
解答 解:由(1)用pH试纸检验,溶液的pH≈7,则不含能水解显酸性或碱性的离子;
(2)向溶液中滴加新制氯水,无气体产生,加入四氯化碳振荡、静置,四氯化碳层呈红棕色,用分液漏斗分液,可知一定含Br-;
(3)向分液后所得的水溶液中加入硝酸钡和稀硝酸的混合液.只有白色沉淀产生,过滤,白色沉淀为BaSO4,则含SO32-;
(4)在滤液中加入硝酸银和稀硝酸的混合液,有白色沉淀产生白色沉淀为AgCl,但(2)中加氯水引入氯离子,
综上所述,肯定有SO32-、Br-,则一定不含Ba2+、S2-、HCO3-、AlO2-,可能含Cl-,由电荷守恒可知一定含阳离子为Na+,
故选C.
点评 本题考查常见离子的检验,为高频考点,把握发生的反应、现象与结论的关系为解答的关键,侧重分析与应用能力的考查,注意(3)中白色沉淀为硫酸钡,题目难度不大.

练习册系列答案
相关题目
12.下列实验能获得成功的是( )
| A. | 苯、溴水、铁粉混合制成溴苯 | |
| B. | 甲烷与氯气光照制得纯净的一氯甲烷 | |
| C. | 用高锰酸钾溶液除去乙烷中的乙烯杂质 | |
| D. | 可以采取蒸馏的方法,分离苯和硝基苯 |
16.2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,下列有关说法正确的是( )
| A. | 丁烷的一氯代物有5种 | B. | 丙烷分子中所有原子共平面 | ||
| C. | 符合通式CnH2n+2的均属于烷烃 | D. | 以上说法均不正确 |
6.下列有关物理量相应的单位表达中,错误的是( )
| A. | 摩尔质量g/mol | B. | 气体摩尔体积L/mol | ||
| C. | 物质的量mol/L | D. | 密度g/cm3 |
 (也可表示为
(也可表示为 )是一种重要的药物中间体,现欲通过如下途径合成:
)是一种重要的药物中间体,现欲通过如下途径合成:

 ;该反应的类型是取代反应或水解反应.
;该反应的类型是取代反应或水解反应. -COOH,则X的结构简式为BrCH2CH2Br.
-COOH,则X的结构简式为BrCH2CH2Br.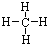 ;(3)O2O=O.
;(3)O2O=O.