题目内容
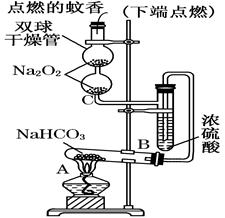
某探究小组采用下图所示装置进行Fe粉与水蒸气的反应。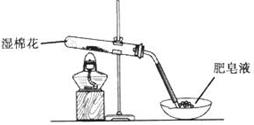
(1)实验前检查装置气密性的方法为________________________________________________________。
(2)检验实验中生成气体的实验操作是_____________________________________________。
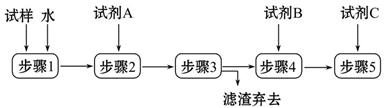
(3)将探究小组分为两组,按题图装置进行对比实验,甲组用酒精喷灯、乙组用酒精灯加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,无气泡 |
| 2 | 取步骤1中溶液,滴加酸性KMnO4溶液 | 紫色褪去 | 紫色褪去 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
①乙组得到的黑色粉末是 。
②甲组步骤1中反应的离子方程式为 。
③乙组步骤4中,溶液变红的原因为 ;溶液褪色可能的原因是 ;验证方法为 。
(1)将装置末端的导管插入盛有水的水槽中,双手捂住试管,导管口有气泡冒出,松开双手,导管内有一段水柱,则装置气密性良好;(2)点燃肥皂泡,有爆鸣声 (3)①FeO②Fe3O4+8H+=2Fe3++ Fe2+ +4H2O ③氯气将Fe2+氧化成Fe3+,Fe3+与SCN-反应溶液呈红色 SCN-被过量氯气氧化 ;向溶液中再加入KSCN溶液,溶液呈红色则说明之前SCN-被过量氯气氧化。
解析试题分析:(1)实验前检查装置气密性的方法为:将装置末端的导管插入盛有水的水槽中,双手捂住试管,导管口有气泡冒出,松开双手,导管内有一段水柱,则装置气密性良好;(2)实验所得的气体为氢气,检验氢气的实验操作是点燃肥皂泡,有爆鸣声;(3)实验所得的物质为FeO或Fe3O4,由于像乙实验所得的溶液中滴加KSCN溶液,无现象,故乙实验中所得的物质为FeO,甲实验中所得的物质为Fe3O4,故①乙组得到的黑色粉末是FeO②Fe3O4与稀盐酸反应的化学方程式为:Fe3O4+8H+=2Fe3++ Fe2+ +4H2O;③乙组步骤4中,溶液变红的原因为氯气将Fe2+氧化成Fe3+,Fe3+与SCN-反应溶液呈红色 ;SCN-被过量氯气氧化;向溶液中再加入KSCN溶液,溶液呈红色则说明之前SCN-被过量氯气氧化。
考点:探究实验,铁与水蒸气的反应。

 阅读快车系列答案
阅读快车系列答案我国化工专家侯德榜发明的侯氏制碱法的化学原理是将二氧化碳通入氨水的氯化钠饱和溶液中,其化学反应方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。
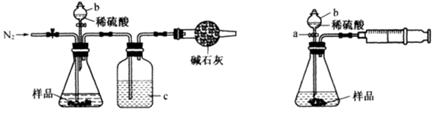
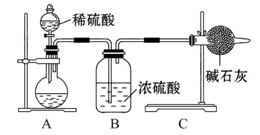
(1)在实验室中利用上述原理从反应所得溶液中分离出碳酸氢钠晶体,应选用下列装置中的 。
(2)实验所得碳酸氢钠晶体中,可能含有的杂质离子有Cl—和NH4+,实验室鉴定Cl—所选用的试剂是、,鉴定另一种杂质离子的方法是 (填序号)。
| A.加水,将湿润的红色石蕊试纸放在试管口 |
| B.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口 |
| C.加氢氧化钠溶液,加热,滴入酚酞试剂 |
| D.加氢氧化钠溶液,加热,滴入紫色石蕊试剂 |
为探究Fe(NO3)2等硝酸盐热分解产物和产物的性质,某化学小组开展如下探究:
【查阅资料】2KNO3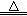 2KNO2+O2↑ Fe(NO3)2
2KNO2+O2↑ Fe(NO3)2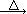 FexOy+NO2↑+O2↑
FexOy+NO2↑+O2↑
实验一:探究Fe(NO3)2热分解固体产物中铁元素的价态。该小组甲同学将分解后的固体产物溶于足量的稀H2SO4得到相应两份溶液,进行以下探究实验。
(1)【提纯猜想】
猜想一:铁元素只显+2价;
猜想二:铁元素 ;
猜想三:铁元素既有+2价又有+3价。
【实验操作】①向一份溶液中滴入KSCN溶液;向另一份溶液中滴入酸性KMnO4稀溶液。
(2)【实验现象】实验① ;实验② 。
(3)【实验结论】猜想二成立,则Fe(NO3)2分解的化学方程式是 。
实验二:
(4)探究Fe(NO3)2热分解气体产物的性质。小组乙同学进行料如下实验,请完成实验空缺部分内容。限选试剂和用品:浓H2SO4溶液、4mol/LNaOH溶液、0.1mol/LBaCl2溶液、带火星的木条、0.1mol/L酸性KMnO4溶液、蒸馏水。
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量Fe(NO3)2固体于试管中,加热分解。 | ,说明分解产生的气体中含有NO2。 |
| 步骤2:将产生的气体依次通过盛有足量 、浓硫酸的洗气瓶, 在最后一个出口检验。 | ,说明分解产生的气体中含O2。 |
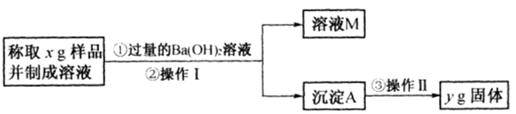
实验三:KNO3中混有Fe(NO3)2,为确定其中铁元素的含量,小组丙同学进行如下实验:①取混合物样品10g,充分加热分解;②将固体产物溶解、过滤,取沉淀进行洗涤、干燥,称得其质量为3.2g。则混合物中铁元素的质量分数为 。(保留三位有效数字,相对原子质量:Fe-56 O-16)

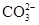 沉淀完全,能否使用氯化钙溶液代替氯化钡溶液?_______ (填“能”或“否”),原因是:_____________________________________。
沉淀完全,能否使用氯化钙溶液代替氯化钡溶液?_______ (填“能”或“否”),原因是:_____________________________________。