题目内容
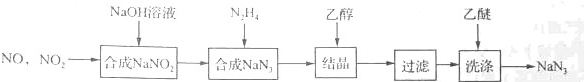
烟气中的NOx是NO和NO2的混合物(不含N2O4).
(1)根据废气排放标准,1m3烟气中最高允许含400mg NOx.若NOx中NO的质量分数为0.85,则1m3烟气中最高允许含NO L(标准状况,保留2位小数).
(2)工业上通常用溶质的质量分数为0.15的Na2CO3溶液(密度为1.16g?mL-1)作为NOx的吸收剂,该碳酸钠溶液的物质的量浓度为 mol?L-1(保留2位小数).
(3)已知:NO+NO2+Na2CO3═2NaNO2+CO2 ①2NO2+Na2CO3═NaNO2+NaNO3+CO2 ②
将1m3含2000mg NOx的烟气用质量分数为0.15的碳酸钠溶液吸收.若吸收率为80%,则吸收后的烟气 (填“符合”或“不符合”)排放标准,其理由是 .
(1)根据废气排放标准,1m3烟气中最高允许含400mg NOx.若NOx中NO的质量分数为0.85,则1m3烟气中最高允许含NO
(2)工业上通常用溶质的质量分数为0.15的Na2CO3溶液(密度为1.16g?mL-1)作为NOx的吸收剂,该碳酸钠溶液的物质的量浓度为
(3)已知:NO+NO2+Na2CO3═2NaNO2+CO2 ①2NO2+Na2CO3═NaNO2+NaNO3+CO2 ②
将1m3含2000mg NOx的烟气用质量分数为0.15的碳酸钠溶液吸收.若吸收率为80%,则吸收后的烟气
考点:氮的氧化物的性质及其对环境的影响,有关混合物反应的计算
专题:计算题,元素及其化合物
分析:(1)根据NO的质量分数计算NO的质量,在根据n=
计算NO的物质的量,根V=nVm计算NO的体积;
(2)根据c=
计算碳酸钠溶液物质的量浓度;
(3)未被被吸收的NOx的质量为2000mg×(1-80%)=400mg,因吸收后烟气总体积减小,NOx含量仍超过400mg/m3.
| m |
| M |
(2)根据c=
| 1000ρw |
| M |
(3)未被被吸收的NOx的质量为2000mg×(1-80%)=400mg,因吸收后烟气总体积减小,NOx含量仍超过400mg/m3.
解答:
解:(1)NO的最大质量为400mg×0.85=340mg,NO的体积为
×22.4L/mol=0.25L,故答案为:0.25;
(2)该碳酸钠溶液物质的量浓度为
mol/L=1.64mol/L,故答案为:1.64;
(3)未被被吸收的NOx的质量为2000mg×(1-80%)=400mg,因吸收后烟气总体积减小,NOx含量仍超过400mg/m3,故不符合,
故答案为:不符合,吸收后烟气总体积减小,NOx含量仍超过400mg/m3.
| 0.34g |
| 30g/mol |
(2)该碳酸钠溶液物质的量浓度为
| 1000×1.16×0.15 |
| 106 |
(3)未被被吸收的NOx的质量为2000mg×(1-80%)=400mg,因吸收后烟气总体积减小,NOx含量仍超过400mg/m3,故不符合,
故答案为:不符合,吸收后烟气总体积减小,NOx含量仍超过400mg/m3.
点评:本题考查物质的量浓度计算、物质含量的有关计算等,难度较大,(3)为易错点,容易忽略体积变化,掌握题干信息和计算方法是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
测得室温下0.1mol?L-1的某酸HA溶液的PH=3,下列叙述错误的是( )
| A、HA是弱酸 |
| B、若升高温度,溶液的PH增大 |
| C、此酸的电离平衡常数约为10-5 |
| D、由HA电离出的c(H+)约为水电离出的c(H+)的108倍 |
以乙炔为原料制取CH2Br-CHBrCl,可行的反应途径是( )
| A、先与Cl2加成,再与Br2加成 |
| B、先与Cl2加成,再与HBr加成 |
| C、先与HCl加成,再与HBr加成 |
| D、先与HCl加成,再与Br2加成 |
“绿色化学”要求不产生副产物,实现零排放.现实验室中要合成一溴乙烷,下列最符合绿色化学要求的是( )
| A、乙烷和溴蒸气在光照下发生反应 |
| B、将乙烯通入溴水中发生反应 |
| C、乙烯与溴化氢在一定条件下反应 |
| D、乙炔与溴化氢在一定条件下反应 |
蒸干下列溶液,能得到该溶质的是( )
| A、NaHCO3溶液 |
| B、KNO3溶液 |
| C、Fe2(SO4)3溶液 |
| D、AlCl3溶液 |