题目内容
经常有人因误食亚硝酸钠(NaNO2)而中毒,原因是NaNO2像食盐一样既有咸味,又有很强毒性.已知亚硝酸钠能发生如下反应:
2NaNO2+4HI═2NO↑+I2+2NaI+2H2O
(1)HI表现的性质是 (填序号)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)当此反应中转移的电子数为0.6mol时,氧化产物的物质的量为 mol.
(3)(提示:HI为强酸)将上述反应改写为离子方程式
(4)上述反应中,氧化性强弱为 > .
2NaNO2+4HI═2NO↑+I2+2NaI+2H2O
(1)HI表现的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)当此反应中转移的电子数为0.6mol时,氧化产物的物质的量为
(3)(提示:HI为强酸)将上述反应改写为离子方程式
(4)上述反应中,氧化性强弱为
考点:氧化还原反应,氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:(1)HI中I元素的化合价部分升高,部分不变,生成盐(NaI);
(2)I元素的化合价由-1升高为0,根据电子与碘的关系计算;
(3)在离子反应方程式中单质、气体、水应保留化学式;
(4)氧化剂的氧化性大于氧化产物的氧化性.
(2)I元素的化合价由-1升高为0,根据电子与碘的关系计算;
(3)在离子反应方程式中单质、气体、水应保留化学式;
(4)氧化剂的氧化性大于氧化产物的氧化性.
解答:
解:(1)由2NaNO2+4HI=2NO+I2+2NaI+2H2O可知,HI中I元素的化合价部分升高,部分不变,生成盐(NaI),则HI体现酸性和还原性,
故答案为:B;
(2)N元素的化合价由+3降低为+2,I元素的化合价由-1升高为0,当生成1mol氧化产物I2时转移2mol电子,已知转移的电子数为0.6mol,则生成的I2为0.3mol;
故答案为:0.3mol;
(3)2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,反应中I2、NO、H2O在改写成离子反应时保留化学式,则离子反应为:2NO2-+4H++2I-═2NO↑+I2+2H2O;
故答案为:2NO2-+4H++2I-═2NO↑+I2+2H2O;
(4)2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,反应中NaNO2为氧化剂,I2为氧化产物,所以氧化性NaNO2>I2;
故答案为:NaNO2、I2.
故答案为:B;
(2)N元素的化合价由+3降低为+2,I元素的化合价由-1升高为0,当生成1mol氧化产物I2时转移2mol电子,已知转移的电子数为0.6mol,则生成的I2为0.3mol;
故答案为:0.3mol;
(3)2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,反应中I2、NO、H2O在改写成离子反应时保留化学式,则离子反应为:2NO2-+4H++2I-═2NO↑+I2+2H2O;
故答案为:2NO2-+4H++2I-═2NO↑+I2+2H2O;
(4)2NaNO2+4HI═2NO↑+I2+2NaI+2H2O,反应中NaNO2为氧化剂,I2为氧化产物,所以氧化性NaNO2>I2;
故答案为:NaNO2、I2.
点评:本题考查氧化还原反应及有关计算,明确常见元素的化合价及反应中元素的化合价变化是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
下列说法中,正确的是( )
| A、工业上制备镁是用电解饱和氯化镁水溶液来完成的 |
| B、硅的化学性质不活泼,在自然界中可以以游离态存在 |
| C、Na2O和Na2O2组成元素相同,且都能与硫酸溶液反应 |
| D、SO2通入新制氯水中,氯水褪色是因为SO2具有漂白性 |
亚氯酸钠(NaClO2)可用作漂白剂,在酸性溶液中因生成亚氯酸而发生分解,分解的化学方程式为5HClO2=4ClO2↑+HCl+2H2O,ClO2是广谱型消毒剂.下列说法正确的是( )
| A、HClO2只是还原剂 |
| B、上述反应中,ClO2是氧化产物 |
| C、上述反应中,1mol HClO2分解转移2mol电子 |
| D、上述反应中,氧化剂与还原剂物质的量之比为1:4 |
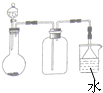
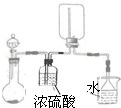
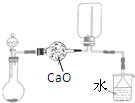

 A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示.请回答下列问题:
A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如图所示.请回答下列问题: