题目内容
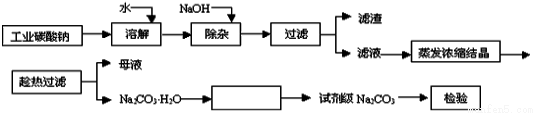
(12分)碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO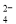 等杂质,提纯工艺路线如下:
等杂质,提纯工艺路线如下:
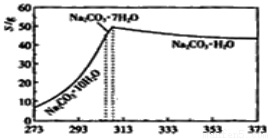
已知碳酸钠的溶解度(S)随温度变化的曲线如图所示:
回答下列问题:
(1)滤渣的主要成分为_________________________。
(2)“趁热过滤”的原因是______________________。
(3)在实验室做Na2CO3·H2O脱水实验,判断其脱水完全的方法是:__________。
(4)生产过程中“母液”____(填“能”或“不能”)循环使用。若不能,其原因是:_________。
(5)已知:① Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g);ΔH1= +532.36 kJ·mol-1
② Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g);ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式_____________________。
(1) 滤渣的主要成分为Mg(OH)2、Fe(OH)3、CaCO3。
(2) “趁热过滤”的原因是使析出的晶体为Na2CO3·H2O,防止因温度过低而析出Na2CO3·10H2O晶体,令后续的加热脱水耗时长。
(3) 连续两次称量的质量差不超过0.1g。
(4) 不能。原因:“母液”中,含有的离子有Ca2+,Na+,Cl-,SO42-,OH-,CO32-,当多次循环后,使用离子浓度不断增大,溶解时会生成CaSO4,Ca(OH)2,CaCO3等沉淀。(若“母液”循环使用,可能出现的问题:溶解时有大量沉淀生成,使Na2CO3损耗且产物Na2CO3混有杂质;)
(5) Na2CO3·H2O(s)==Na2CO3(s)+ H2O(g); △H= +58.73kJ/mol
【解析】
试题分析:(1)向含有杂质离子Ca2+、Mg2+、Fe3+、Cl-和SO42-等的碳酸钠溶液中加入NaOH溶液发生反应产生Mg(OH)2、Fe(OH)3、CaCO3沉淀;(2) “趁热过滤”的原因是是使析出的晶体为Na2CO3·H2O,防止因温度过低而析出Na2CO3·10H2O晶体,令后续的加热脱水耗时长。(3)在实验室做Na2CO3·H2O脱水实验,判断其脱水完全的方法是 连续加热,冷却后称量固体的质量,两次称量的质量差不超过0.1g。(4)将产生的沉淀过滤出去,得到的滤液中含有Ca2+,Na+,Cl-,SO42-,OH-,CO32-,当多次循环后,使用离子浓度不断增大,溶解时会生成CaSO4,Ca(OH) 2,CaCO3等沉淀。所以生产过程中“母液”不能循环使用;(5)①-②,整理可得: Na2CO3·H2O(s)==Na2CO3(s)+ H2O(g); △H= +58.73kJ/mol。
考点:考查物质的提纯、混合物的分离方法、物质的循环利用、热化学方程式的书写的知识。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案