��Ŀ����
��ͼ��ʾ����ԲȦ�ཻ�IJ��ֱ�ʾԲȦ�ڵ�����������ķ�Ӧ����֪�Ƽ�������������ʵ�����Ϊ0.1 mol��ˮ������Ϊ100 g������˵����ȷ����( )
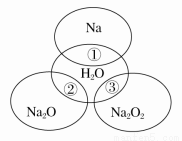
A�� ��Ӧ������ܲ���0.05 mol O2
B�� ��Ӧ�ٵ����ӷ���ʽΪNa��2H2O==Na����2OH����H2��
C�� Na2O2������������Ŀ֮��Ϊ1��1
D�� �١��ڡ��۳�ַ�Ӧ��������Һ�����ʵ�������������>��>��
A
��������
���������A�� Na2O2��ˮ��Ӧ����ʽ�ǣ�2Na2O2+2H2O=4NaOH+ O2����0.1mol��Na2O2��Ӧ����ˮ0.1mol(��1.8g),��������0.05 mol����˷�Ӧ������ܲ���0.05 mol O2����ȷ��B�� ��ɲ��غ㣬��Ӧ�ٵ����ӷ���ʽΪ2Na��2H2O==2Na����2OH����H2��������C�� Na2O2������������Ŀ֮��Ϊ1��2������D�� �١��ڡ��۳�ַ�Ӧ��������Һ�����ʵ����ʵ����ֱ���0.1mol��0.2mol��0.2mol�����ĵ�ˮ����ͬ���������ʵ���������������<��=��,����
���㣺�����Ƽ���������Ľṹ������ˮ������Ӧ��ԭ�������������ıȽϵ�֪ʶ��

��ϰ��ϵ�д�
 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д�
�����Ŀ

 ��Ϊ4A�ͷ���ɸ����Na+��Ca2+ȡ��ʱ���Ƶ�5
��Ϊ4A�ͷ���ɸ����Na+��Ca2+ȡ��ʱ���Ƶ�5 �ͷ���ɸ����Na+��K+ȡ��ʱ���Ƶ�3
�ͷ���ɸ����Na+��K+ȡ��ʱ���Ƶ�3 )Ӧ��ѡ�� �ͷ���ɸ
)Ӧ��ѡ�� �ͷ���ɸ 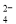 �����ʣ��ᴿ����·�����£�
�����ʣ��ᴿ����·�����£�
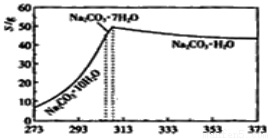

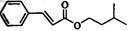 ����һ�����ϣ�һ�ֺϳ�·�����£�
����һ�����ϣ�һ�ֺϳ�·�����£�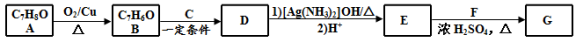
 ��
��