题目内容
7.如图每一方格表示一种物质.通常状况下,A、C均为无色气体,B为无色液体.请填写下列空白: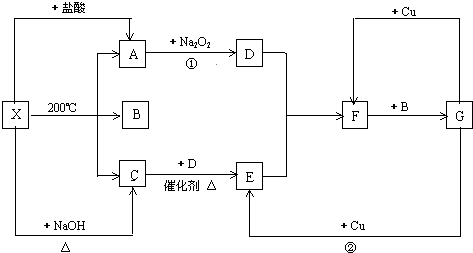
(1)物质X可以是(NH4)2CO3或NH4HCO3,C是NH3,F是NO2;
(2)反应①的化学方程式是2Na2O2+2CO2═2Na2CO3+O2;
(3)反应②的离子方程式是3Cu+2NO3-+8H+=3Cu2++4H2O+2NO↑.
分析 X既能与盐酸反应,又能与NaOH反应,都生成气体,应为弱酸铵盐,则C为NH3,气体A能与过氧化钠反应,故A为CO2,则A应为(NH4)2CO3或NH4HCO3,B为H2O,结合转化关系可知,D为O2,E为NO,F为NO2,G为HNO3,结合物质的性质进行解答.
解答 解:X既能与盐酸反应,又能与NaOH反应,都生成气体,应为弱酸铵盐,则C为NH3,气体A能与过氧化钠反应,故A为CO2,则A应为(NH4)2CO3或NH4HCO3,B为H2O,结合转化关系可知,D为O2,E为NO,F为NO2,G为HNO3,
(1)由上述分析可知,物质X可以是(NH4)2CO3或NH4HCO3,C是NH3,F是NO2,故答案为:(NH4)2CO3或NH4HCO3;NH3;NO2;
(2)反应①的化学方程式是:2Na2O2+2CO2═2Na2CO3+O2,
故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(3)反应②的离子方程式是:3Cu+2NO3-+8H+=3Cu2++4H2O+2NO↑,
故答案为:3Cu+2NO3-+8H+=3Cu2++4H2O+2NO↑.
点评 本题考查无机物的推断,X能与酸、碱反应生成气体A、C为推断突破口,然后利用转化关系推出各物质,题目难度中等.

练习册系列答案
相关题目
17.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)这些元素中,化学性质最不活泼的是Ar(填元素符号,下同).
(2)最高价氧化物的水化物中,酸性最强的化合物的化学式:HClO4,碱性最强的化合物的电子式: .
.
(3)最高价氧化物是两性氧化物的元素是Al.
(4)用电子式表示元素④与⑥形成化合物的过程: .
.
(5)①与⑦形成的化合物的电子式: ,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(2)最高价氧化物的水化物中,酸性最强的化合物的化学式:HClO4,碱性最强的化合物的电子式:
 .
.(3)最高价氧化物是两性氧化物的元素是Al.
(4)用电子式表示元素④与⑥形成化合物的过程:
 .
.(5)①与⑦形成的化合物的电子式:
 ,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
,该化合物是由极性(填“极性”或“非极性”)共价键形成的.
18.下列物质属于纯净物的是( )
| A. | 空气 | B. | 氨水 | C. | 磁铁矿 | D. | 冰水共存物 |
12.Na[Al(OH)4]向溶液中持续通入一种气体,开始时产生沉淀,随后沉淀又逐渐溶解,该气体是( )
| A. | HCl | B. | CO2 | C. | NH3 | D. | CO |
16.下列化学反应的离子方程式正确的是( )
| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓ | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |
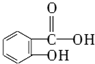 ,俗名水杨酸.
,俗名水杨酸. .
.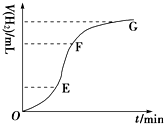 现欲用纯净的锌粒与稀盐酸反应制取H2,请回答:
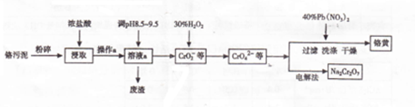
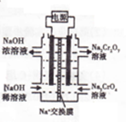
现欲用纯净的锌粒与稀盐酸反应制取H2,请回答: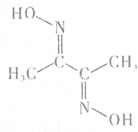 铁、钴、镍等金属及其化合物在工业上有重要用途.请回答:
铁、钴、镍等金属及其化合物在工业上有重要用途.请回答: