题目内容
15.下列关于葡萄糖的叙述,错误的是( )| A. | 化学式为:C6H12O6 | B. | 能发生酯化反应和银镜反应 | ||
| C. | 易溶于水,有甜味,属于碳水化合物 | D. | 能发生水解反应 |
分析 A.葡萄糖化学式为:C6H12O6;
B.葡萄糖中含有醛基和羟基;
C.葡萄糖易溶于水,有甜味;
D.葡萄糖是单糖.
解答 解:A.葡萄糖化学式为:C6H12O6,故A正确;
B.葡萄糖中含有醛基和羟基,能发生酯化反应和银镜反应,故B正确;
C.葡萄糖易溶于水,有甜味,属于碳水化合物,故C正确;
D.葡萄糖是单糖,不能发生水解,故D错误.
故选D.
点评 本题考查葡萄糖的性质和用途,注意葡萄糖中含有醛基和羟基,能发生酯化反应和银镜反应,题目难度不大.

练习册系列答案
相关题目
5.下列物质不属于强电解质的是( )
| A. | 硫酸 | B. | 醋酸 | C. | 氢氧化钡 | D. | 硫酸钡 |
6.下列说法正确的是( )
| A. | FeCl3溶液需存放在加有少量铁粉的试剂瓶中,防止变质 | |
| B. | 食盐水中Ca2+、SO42-等杂质的去除,应先加Na2CO3溶液,后加BaCl2溶液 | |
| C. | 用四氯化碳来萃取碘水中的I2,有机层应从分液漏斗的下端放出 | |
| D. | 用BaCl2溶液来检验暴露在空气中的Na2SO3样品是否变质 |
3.下列除去有关物质中杂质的方案中,正确的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质使用的试剂 | 除去杂质的方法 |
| A | Cl2气(HCl气) | NaOH溶液,浓硫酸 | 洗气 |
| B | NH4Cl溶液(FeCl3) | NaOH溶液 | 过滤 |
| C | Na2CO3固体(NaHCO3) | ---- | 灼烧 |
| D | I2 (H2O) | CCl4 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
20.下列有关Na2CO3溶液中微粒的物质的量浓度关系正确的是 ( )
| A. | 在0.1mol•L-1Na2CO3溶液中:c(Na+)>c(CO32-)>c(H2CO3)>c(HCO3-) | |
| B. | 在0.1mol•L-1Na2CO3溶液中:c(OH-)-c(H+)═c(HCO3-)+c(H2CO3) | |
| C. | 在0.1mol•L-1Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)>c(H CO3-)>c(H+) | |
| D. | 在0.1mol•L-1Na2CO3溶液中:c(Na+)+c(H+)═c(CO32-)+c(OH-)+c(H CO3-) |
7.丰富多彩的颜色变化增添了化学实验的魅力,下列有关反应颜色变化的叙述中,正确的是:①氯气通入湿润的蓝色石蕊试纸后→红色 ②无水硫酸铜遇水蒸气→蓝色 ③蔗糖中加入浓硫酸搅拌→白色 ④SO2通入高锰酸钾溶液中→紫红色褪去 ⑤氨气通入酚酞溶液中→红色( )
| A. | ①②③④ | B. | ①②④⑤ | C. | ②④⑤ | D. | ②③④ |
4.下表中所示实验装置的图示或操作中,不能达到实验目的是( )
| A. | 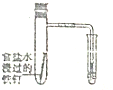 验证铁的析氢腐蚀 | B. | 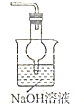 吸收SO2 | ||
| C. | 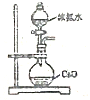 制取少量氨气 | D. | 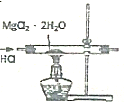 制取无水MgCl2 |
8.2015年10月5日,中国药学家屠呦呦因发现了青蒿素和双氢青蒿素获2015年诺贝尔生理学或医学奖.青蒿素分子式C15H22O5,含有7个手性碳原子.下列化合物中含有不止一个手性碳原子的是( )
| A. | CH3CHO | B. | CH2OH(CHOH)4CHO | C. | CH3CH2CH2OH | D. | CH3CH(OH)COOH |
 数十年来,化学工作者对碳的氧化物和氢化物做了广泛深入的研究并取得了一些
数十年来,化学工作者对碳的氧化物和氢化物做了广泛深入的研究并取得了一些 .
.