题目内容
6.有A、B、C、D、E五瓶透明溶液,分别是HCl、BaCl2、NaHSO4、Na2CO3、AgNO3中的一种.已知:①A与B反应有气体生成;②B与C反应有沉淀生成;③C与D反应有沉淀生成;④D与E反应有沉淀生成;⑤A与E反应有气体生成;⑥在②和③的反应中生成的沉淀是同一种物质.请填空:(1)在②和③的反应中,生成的沉淀物质的化学式是AgCl;E是NaHSO4.
(2)写出⑤反应的离子方程式是2H++CO32-═CO2↑+H2O.
分析 根据⑥“在②和③的反应中生成的沉淀是同一种物质”这一信息可知,B与D中必然含有相同的离子,容易推断出它们是HCl和BaCl2,都可与银离子反应生成AgCl沉淀;因此,C必然是AgNO3;再根据①,A与B反应有气体生成,推断B一定是HCl,那么,D是BaCl2,A是Na2CO3,剩余的一种物质,即NaHSO4就是E,结合对应物质的性质以及题目要求解答该题.
解答 解:根据⑥“在②和③的反应中生成的沉淀是同一种物质”这一信息可知,B与D中必然含有相同的离子,容易推断出它们是HCl和BaCl2,都可与银离子反应生成AgCl沉淀;因此,C必然是AgNO3;再根据①,A与B反应有气体生成,推断B一定是HCl,那么,D是BaCl2,A是Na2CO3,剩余的一种物质,即NaHSO4就是E,
(1)由以上分析可知在②和③的反应中,生成的沉淀物质是AgCl,E为NaHSO4,故答案为:AgCl;NaHSO4;
(2)A是Na2CO3,E为NaHSO4,Na2CO3与NaHSO4反应生成CO2和H2O,反应的离子方程式是2H++CO32-═CO2↑+H2O,故答案为:2H++CO32-═CO2↑+H2O.
点评 本题考查物质的检验和鉴别,为高考常见题型,侧重于学生的分析能力的考查,注意把握元素化合物知识,学习中注意相关基础知识的积累,根据反应现象进行推断,难度不大.

练习册系列答案
相关题目
16.2009年诺贝尔物理奖授予了“光导纤维之父”高锟.光导纤维的成分是( )
| A. | Si | B. | 石墨 | C. | SiO2 | D. | 纳米硅 |
14.下列说法正确的是( )
| A. | 22.4升氧气中一定含有阿伏加德罗常数个氧分子 | |
| B. | 1摩氧气的质量是32克 | |
| C. | 1摩氧气与1摩二氧化碳中的原子个数相等 | |
| D. | H2SO4的摩尔质量是98克 |
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下22.4LHF中所含电子数为10NA | |
| B. | 100mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.6NA | |
| C. | 1mol•L-1 Na2CO3溶液中,CO32-的数目小于NA | |
| D. | 1 mol CH5+中含有的电子数目为10NA |
11.化学在人类社会发展中起着重要的作用,请你分析下列四个选项中化学学科不涉及的研究领域是( )
| A. | 开发新的能源 | B. | 合成新的物质 | ||
| C. | 研究物体运动规律 | D. | 防治环境污染 |
16.能在水溶液中大量共存的离子组是( )
| A. | H+、Fe3+、SO42-、I- | B. | Na+、NH4+、CO32-、NO3- | ||
| C. | Ag+、K+、Cl-、SO42- | D. | K+、AlO2-、Cl-、HCO3- |
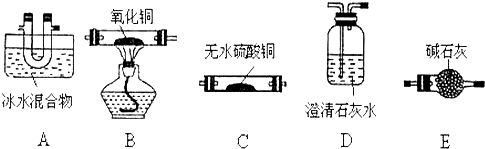
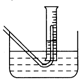 Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,做如下实验(假设杂质不参加反应)
Na2O2与水的反应实际是Na2O2+2H2O═2NaOH+H2O2,反应放热使部分H2O2受热分解:2H2O2═2H2O+O2↑.为了测定某过氧化钠固体的纯度,做如下实验(假设杂质不参加反应)