题目内容
在标准状况下,将1g氦气,11g二氧化碳和4g氧气混合,求该混合气体的体积.
考点:物质的量的相关计算
专题:计算题
分析:标况下,气体摩尔体积为22.4L/mol,根据V=nVm计算混合气体体积.
解答:
解:标况下,气体摩尔体积为22.4L/mol,二氧化碳的物质的量=
=0.25mol、氧气的物质的量=
=0.125mol,氦气的物质的量=
=0.25mol,所以混合气体的物质的量=(0.25+0.125+0.25)mol=0.625mol,V=nVm=0.625mol×22.4L/mol=14L,
答:混合气体的体积为14L.
| 11g |
| 44g/mol |
| 4g |
| 32g/mol |
| 1g |
| 4g/mol |
答:混合气体的体积为14L.
点评:本题考查了物质的量的有关计算,灵活运用基本公式来分析解答,氦气是单原子分子,为易错点.

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、凡是能电离出H+的化合物均属于酸 |
| B、由一种元素组成的物质一定是单质 |
| C、纯碱从物质的分类看不属于碱 |
| D、盐类物质一定含有金属离子 |
已知汽车尾气无害化处理反应为2NO(g)+2CO(g)?N2(g)+2CO2(g)下列说法不正确的是( )
| A、增大压强正反应速率增大,逆反应速率减小,平衡右移 |
| B、使用高效催化剂可有效提高正反应速率 |
| C、反应达到平衡后,N0的反应速率保持恒定 |
| D、单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 |
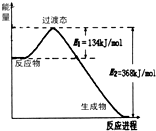 (1)在25℃、101kPa下,1g甲烷完全燃烧生成CO2和液态H2O,放出55kJ的热量,写出表示甲烷燃烧热的热化学方程式:
(1)在25℃、101kPa下,1g甲烷完全燃烧生成CO2和液态H2O,放出55kJ的热量,写出表示甲烷燃烧热的热化学方程式: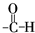
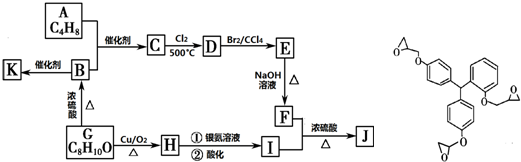
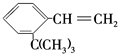 滴入溴水后生成产物的结构简式为
滴入溴水后生成产物的结构简式为