题目内容
某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol·L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响;) |
| ② | ||||
| ③ | ||||
| ④ |
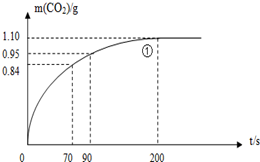
(2)实验①中CO2质量随时间变化的关系见下图:
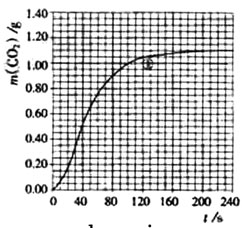
依据反应方程式![]() CaCO3+HNO3=
CaCO3+HNO3=![]() Ca(NO3)2+
Ca(NO3)2+![]() CO2↑+
CO2↑+![]() H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程)。
H2O,计算实验①在70-90 s范围内HNO3的平均反应速率(忽略溶液体积变化,写出计算过程)。
(3)请在答题卡的框图中,画出实验②、③和④中CO2质量随时间变化关系的预期结果示意图。
(1)
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol·L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | ⑴实验①和②探究HNO3浓度对该反应速率的影响; ⑵实验①和③探究温度对该反应速率的影响。 ⑶实验①和④探究大理石规格(粗、细)对该反应的影响。 |
| ② | 298 | 粗颗粒 | 1.00 | |
| ③ | 308 | 粗颗粒 | 2.00 | |
| ④ | 298 | 细颗粒 | 2.00 |
(2)
m(CO2)0.95-0.85=0.1g
n(HNO3)0.1/22=1/220mol
△c(HNO3)=2/11 mol/L
t=90-70=20s
v(HNO3)=△c(HNO3)/t == 1/110 mol·L-1·S-1
(3)作图略
解析:
(2)70至90S,CO2生成的质量为:m(CO2)0.95-0.85=0.1g
根据方程式比例,可知消耗HNO3的物质的量为:n(HNO3)0.1/22=1/220mol
溶液体积为25ml=0.025L,所以HNO3减少的浓度△c(HNO3)=2/11 mol/L
反应的时间t=90-70=20s
所以HNO3在70-90S范围内的平均反应速率为
v(HNO3)=△c(HNO3)/t == 1/110 mol·L-1·S-1
(3)作图要点:因为实验①HNO3与大理石恰好完全反应;
实验②中,HNO3不足量,纵坐标对应的每一个值均为原来的1/2;
实验③④的图象类似,恰好完全反应,但反应条件改变,升高温度与大理石细颗粒增大表面积可加快反应速率。所以图象曲线斜率变大,平衡位置纵坐标与实验①相同。

 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验编号 | T/K | 大理石规格 | HNO3浓度/mol?L-1 | 实验目的 |
| ① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 (Ⅲ)实验①和 |
| ② | ||||
| ③ | ||||
| ④ |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
(3)预期实验结果是(比较三组实验速率的快慢,用代号)
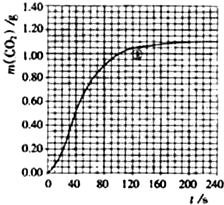
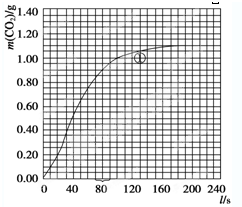
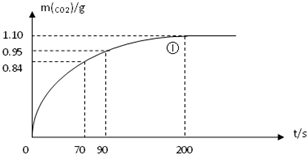
 某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00mL,大理石用量为10.00g.
某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素.所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00mL,大理石用量为10.00g.