题目内容
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示.其中Y所处的周期序数与族序数相等.下列说法正确的是( )
| X | |||
| Y | Z | W |
| A、原子半径:Y<Z<W |
| B、气态氢化物的稳定性:X>Z |
| C、W的最高价氧化物与水反应形成的化合物是离子化合物 |
| D、X的气态氢化物的水溶液能与Y的最高价氧化物对应水化物发生反应 |
考点:位置结构性质的相互关系应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:Y所处的周期序数与族序数相等,短周期元素,则Y为第三周期第ⅢA族元素,即Y为Al,由元素的位置可知,Z为Si,X为N,W为S,以此来解答.
解答:
解:Y所处的周期序数与族序数相等,短周期元素,则Y为第三周期第ⅢA族元素,即Y为Al,由元素的位置可知,Z为Si,X为N,W为S,
A.同周期原子半径从左向右减小,则原子半径为Y>Z>W,故A错误;
B.非金属性X>Z,则气态氢化物的稳定性:X>Z,故B正确;
C.W为S,W的最高价氧化物与水反应形成的化合物是硫酸,只含共价键,属于共价化合物,故C错误;
D.X为N,X的气态氢化物的水溶液氨水,不能与Y的最高价氧化物氢氧化铝反应,故D错误;
故选B.
A.同周期原子半径从左向右减小,则原子半径为Y>Z>W,故A错误;
B.非金属性X>Z,则气态氢化物的稳定性:X>Z,故B正确;
C.W为S,W的最高价氧化物与水反应形成的化合物是硫酸,只含共价键,属于共价化合物,故C错误;
D.X为N,X的气态氢化物的水溶液氨水,不能与Y的最高价氧化物氢氧化铝反应,故D错误;
故选B.
点评:本题考查位置、结构、性质的应用,为高频考点,把握短周期元素的位置及Y的周期序数与族序数相等为解答的关键,侧重分析推断能力的考查,题目难度不大.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
用如图所示装置进行下列实验,能达到实验目的是( )
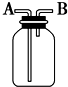

| A、瓶中盛有适量浓H2SO4,从A口进气来干燥NH3 |
| B、从B口进气,用排空气法收集CO2 |
| C、瓶中盛满水,从B口进气,用排水法收集NO2 |
| D、瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量生成H2的体积 |
某同学量取50ml 0.5mol/LNaOH溶液和30ml 0.5mol/L H2SO4溶液做中和热实验,测得中和热数据比57.3kJ?mol-1大,其原因可能是( )
| A、实验装置保温、隔热效果差 |
| B、量取NaOH溶液的体积时仰视读数 |
| C、分多次把NaOH溶液倒入盛有硫酸的小烧杯中 |
| D、用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
下列图示实验合理的是( )
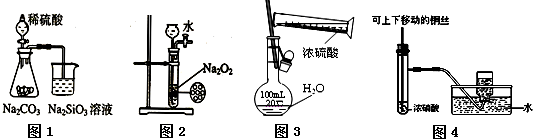

| A、图1为证明非金属性强弱:S>C>Si |
| B、图2为制备少量氧气 |
| C、图3为配制一定浓度硫酸溶液 |
| D、图4为制备并收集少量NO2气体 |
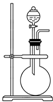 如图是实验室制取某些气体的装置.
如图是实验室制取某些气体的装置.

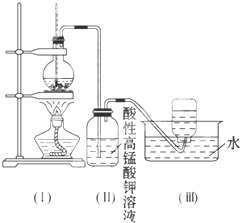 如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯:CH3CH2OH
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯:CH3CH2OH