题目内容
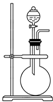 如图是实验室制取某些气体的装置.
如图是实验室制取某些气体的装置.(1)该制气装置在加入反应物前,应事先进行的操作是
(2)若用该装置制取O2,反应物除了可选择二氧化锰和
(3)利用该装置还可制取
(4)此装置中加入漂白粉和浓盐酸也可以制取Cl2.
①写出该反应的离子方程式:
②若使用在空气中放置的漂白粉和浓盐酸发生反应,则制取的Cl2中可能含有的杂质为
考点:实验装置综合
专题:实验设计题
分析:(1)该装置在加入反应物前,先检查装置气密性;
(2)该装置为固液不加热装置,可以用过氧化氢和二氧化锰,或水与过氧化钠反应制备氧气;
(3)该装置为固液不加热装置,结合选项分析;
(4)①酸性条件下次氯酸根离子能氧化氯离子生成氯气;
②漂白粉变质会生成碳酸钙.
(2)该装置为固液不加热装置,可以用过氧化氢和二氧化锰,或水与过氧化钠反应制备氧气;
(3)该装置为固液不加热装置,结合选项分析;
(4)①酸性条件下次氯酸根离子能氧化氯离子生成氯气;
②漂白粉变质会生成碳酸钙.
解答:
解:(1)该装置在加入反应物前,为了防止漏气,应首先检查装置气密性,故答案为:检查装置气密性;
(2)该装置为固液不加热装置,可以用二氧化锰催化过氧化氢分解生成氧气,水与过氧化钠反应生成氢氧化钠和氧气,故答案为:过氧化氢;Na2O2;
(3)该装置为固液不加热装置,
a.用锌与稀硫酸反应制备H2 ,可以选用该装置,故a选;
b.用盐酸和石灰石制备CO2 ,可以选用该装置,故b选;
c.用生石灰与浓氨水制备NH3,可以选用该装置,故c选;
故答案为:abc;
(4)①酸性条件下次氯酸根离子能氧化氯离子生成氯气,则该反应的离子方程式:ClO-+Cl-+2H+=Cl2↑+H2O,故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
②漂白粉变质会生成碳酸钙,在空气中放置的漂白粉含有少量的碳酸钙,则在空气中放置的漂白粉和浓盐酸发生反应,制取Cl2中可能含有的杂质为CO2,故答案为:CO2.
(2)该装置为固液不加热装置,可以用二氧化锰催化过氧化氢分解生成氧气,水与过氧化钠反应生成氢氧化钠和氧气,故答案为:过氧化氢;Na2O2;
(3)该装置为固液不加热装置,
a.用锌与稀硫酸反应制备H2 ,可以选用该装置,故a选;
b.用盐酸和石灰石制备CO2 ,可以选用该装置,故b选;
c.用生石灰与浓氨水制备NH3,可以选用该装置,故c选;
故答案为:abc;
(4)①酸性条件下次氯酸根离子能氧化氯离子生成氯气,则该反应的离子方程式:ClO-+Cl-+2H+=Cl2↑+H2O,故答案为:ClO-+Cl-+2H+=Cl2↑+H2O;
②漂白粉变质会生成碳酸钙,在空气中放置的漂白粉含有少量的碳酸钙,则在空气中放置的漂白粉和浓盐酸发生反应,制取Cl2中可能含有的杂质为CO2,故答案为:CO2.
点评:本题考查了气体的制备、氯元素及其化合物的性质,侧重于实验装置和实验原理的考查,题目难度不大,注意漂白粉在空气中会生成碳酸钙.

练习册系列答案
相关题目
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示.其中Y所处的周期序数与族序数相等.下列说法正确的是( )
| X | |||
| Y | Z | W |
| A、原子半径:Y<Z<W |
| B、气态氢化物的稳定性:X>Z |
| C、W的最高价氧化物与水反应形成的化合物是离子化合物 |
| D、X的气态氢化物的水溶液能与Y的最高价氧化物对应水化物发生反应 |
点燃的镁条伸入盛有下列气体的集气瓶中,能继续燃烧的是( )
①Cl2 ②O2 ③CO2 ④水蒸气.
①Cl2 ②O2 ③CO2 ④水蒸气.
| A、① | B、①② | C、①②③ | D、①②④ |

 某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出).
某研究性学习小组为研究Cu与浓H2SO4的反应,设计如下实验探究方案(装置中的固定仪器和酒精灯均未画出). (1)可逆反应N2(g)+3H2(g)2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为
(1)可逆反应N2(g)+3H2(g)2NH3(g)是一个放热反应,有甲乙两个完全相同的容器,向甲容器中加入1molN2和3molH2在一定条件下,达到平衡时放出的热量为Q1,相同条件下,向乙容器中加入2molNH3,达到平衡时,吸收的热量为Q2,已知Q2=4Q1,则甲容器中H2的转化率为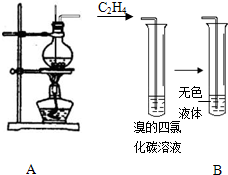 某学习小组用如图所示装置进行验证乙醇和浓硫酸混合加热后是否有乙烯生成的实验.
某学习小组用如图所示装置进行验证乙醇和浓硫酸混合加热后是否有乙烯生成的实验.